题目内容
【题目】NaCl是一种重要原料,其生产与应用如下图所示。下列说法错误的是
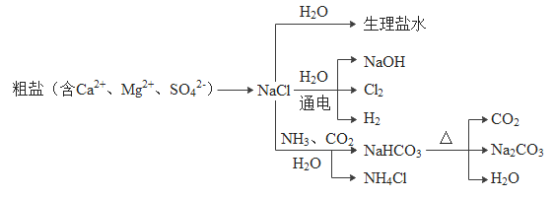
A.由粗盐制NaCl时,除杂试剂的滴加顺序可依次为过量的NaOH、Na2CO3、BaCl2溶液
B.配制一定溶质质量分数的生理盐水主要步骤为计算、称量、溶解、转移、装瓶贴标签
C.上述图示转化反应中各元素的化合价都没有发生变化
D.由NaCl制备Na2CO3过程中可循环使用的物质是CO2和H2O
【答案】AC
【解析】
A、镁离子用氢氧根离子沉淀,加入过量的氢氧化钠溶液可以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡,故选项说法错误;
B、配制一定溶质质量分数的生理盐水,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠和量取水,最后进行溶解、转移、装瓶贴标签,故选项说法正确;
C、上述图示转化反应中,存在化合物与单质之间的转化,一定有元素的化合价发生变化,故选项说法错误;
D、既是反应物,也是生成物的物质但不是要生产的产品,可以循环使用,由NaCl制备Na2CO3过程中可循环使用的物质是CO2和H2O,故选项说法正确。
故选AC。

【题目】化学兴趣小组的同学欲用如图所示实验装置,通过实验探究质量守恒定律,根据实验目的,两位同学用了不同的药品进行实验,结果如下表所示:
所用药品 | 实验前后天平是否平衡 | |
小景 | 氯化钠溶液、硝酸钾溶液 | 平衡 |
小波 | 碳酸钙、稀盐酸 | 不平衡 |
(1)小景同学的天平一直平衡,他认为他的实验验证了质量守恒定律,但在小组讨论时,被同学指出设计错误,原因是_____。
(2)小波同学的实验中天平不平衡,你认为该反应是否_____(填“符合”、“不符合”之一)质量守恒定律,欲使反应前后天平平衡,可对该装置做的改进方法是_____
(3)化学反应前后,下列诸项中肯定没有变化的是_____(填A、B、C、D之一)
①原子的数目 ②分子的数目 ③元素的种类④原子的种类 ⑤物质的种类 ⑥分子的种类
A 只有①④⑥ B 只有①③④ C 只有①②④ D 只有②③⑥
(4)小玉同学做完了质量守恒定律的探究实验后,又欲测定一瓶标签破损的稀硫酸的溶质质量分数。她取了50g稀硫酸样品,逐滴加入10%的氢氧化钠溶液,用pH计测定溶液中pH变化如图所示,试回答:
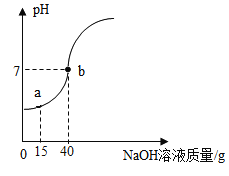
①当滴入氢氧化钠溶液15g时(即图中a点,烧杯内溶液中含有的溶质有_____、_____(写化学式)。
②计算所测稀硫酸的溶质质量分数_____(计算结果精确至0.1%)。