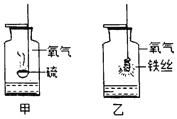
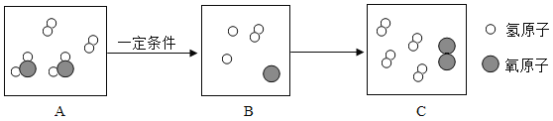
��Ŀ����
����Ŀ��ʵ�������ⶨһƿ��ǩ�����ϡ���������ʵ�������������ȡ10gϡ������Ʒ����5%��NaOH��Һ��μ��뵽��Ʒ�У��ӱ߽��裬����NaOH��Һ�ļ��룬��ҺpH�ı仯�����ͼ��ʾ�����������㣺

��1��a����Һ�к��е�������_____��
��2����pH��7ʱ����������������Һ��NaOH����Ϊ_____g��
��3������ϡH2SO4�����ʵ�����������_____
��4������ǡ����ȫ��Ӧʱ������Һ����������������_____
���𰸡�Na+��H+��SO42- 0.8 ϡH2SO4����������������9.8%�� ǡ����ȫ��Ӧʱ������Һ����������������5.5%��
��������
��1����ͼʾ��֪����a��ʱ��Һ��pHС��7��˵�������NaOH��ȫ��Ӧ����ʣ������ᣬ���ԣ���Һ�к��е�����Ϊ��Na+��H+��SO42-��
��2����ͼʾ��֪������Һ��pH����7�����ĵ�NaOH��Һ������Ϊ16g�����ʵ�����Ϊ��16g��5%=0.8g��
��3��10gϡ������Ʒ����H2SO4������Ϊx�����ɵ������Ƶ�����Ϊy
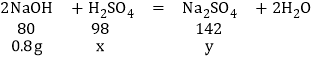
![]() ��ã�x=0.98g y=1.42g
��ã�x=0.98g y=1.42g
ϡH2SO4��������������Ϊ��![]() ��100%=9.8%��
��100%=9.8%��
��4��ǡ����ȫ��Ӧʱ������Һ����������������![]() ��100%��5.5%��
��100%��5.5%��

����Ŀ��ij��ȤС���ͬѧ���֣��ϸ�����ʵ���õ�����������Һ����������ƿ������ƿ��Һ��û�б����أ�ͬѧ����һ̽���������������һ����룮
���������ϣ��Ȼ�����Һ�����ԣ�
��������룩����һ������Һû�б��ʣ�
�����������Һ���ֱ��ʣ�
������������Һ_____���ʣ�
��ʵ����֤��
ʵ�鲽�� | ʵ������ | ʵ����� |
��ȡ��������Һ���Թ��У������еμӹ������Ȼ�����Һ�� | ���ɰ�ɫ���� | ����_____������ |
�ھ��ã����ϲ���Һ�еμӷ�̪��Һ�� | _____ | ��������� |
�����۽�����
��1������ٵμӹ������Ȼ�����Һ��Ŀ����_____��
��2����ͬѧ���������������Һ�����Ȼ�����Һ��ͬ����ʵ�飬Ҳ�ܿ�����ͬ�����ó���ͬ�Ľ��ۣ���ͬ�����Ĺ۵���Ϊʲô��_____��
����˼���������Ƴ��ڷ��ñ��ʵ�ԭ����_____���û�ѧ����ʽ��ʾ���������������Ӧ_____���森