题目内容
【题目】科学探究是学习化学重要而有效的学习方法。某校化学兴趣小组的同学以“酸碱中和反应”为课题进行探究。小宇同学向烧杯中的氢氧化钠溶液中滴加稀硫酸,一会儿后发现忘了滴加酸碱指示剂,于是他停止滴加稀硫酸。同学们纷纷对实验后烧杯中溶液中含有哪些溶质展开了讨论。
(提出问题)实验后的烧杯中溶质含有哪些物质?
(提出猜想)猜想一:溶质中只有Na2SO4;
猜想二:溶质中可能是Na2SO4和NaOH;
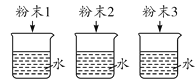
猜想三:溶质中可能是_____。
(查阅资料)Na2SO4溶液呈中性。
(实验探究)小宇同学设计如下的实验方案
方法步骤 | 实验现象 | 实验结论 | |
方案一 | 取少量烧杯中的溶液于洁净的试管中,滴入几滴无色酚酞溶液 | 溶液不变红色 | 猜想一正确 猜想二不正确 |
方案二 | 取少量烧杯中的溶液于洁净的试管中,滴加BaCl2溶液 | 出现白色沉淀 | 猜想三正确 |
方案三 | 取少量烧杯中的溶液于洁净的试管中,加入少量的黑色CuO粉末,振荡 | _____ | 猜想三正确 |
(方案评价)同学们对小宇上述的方案讨论后认为:
①方案一存在缺陷,该方案不能证明猜想一是正确的,其原因是_____。
②方案二也不能证明猜想三是正确的,理由是_____。
③同学们经过讨论,一致认为方案三能够证明猜想三是正确的,并讨论除此方案外,还可以向烧杯的溶液中加入活泼金属、碳酸盐等物质进行证明。
(实验反思)在分析化学反应后所得物质成分时,还需考虑反应物的用量。
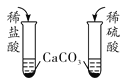
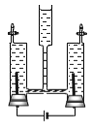
(学科渗透)如图1所示,小宇同学在进行溶液导电性的实验时,将电极两端插入稀H2SO4中。闭合开关,小灯泡正常发光,然后逐滴向稀H2SO4中加入Ba(OH)2溶液至过量,请推测小灯泡的发光情况为_____;发生反应的化学方程式是_____。

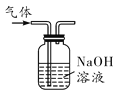
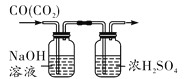
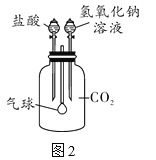
(反思应用)利用如图2所示装置来验证CO2气体的性质,要证明CO2与NaOH溶液能够发生反应,可先加氢氧化钠溶液,再加盐酸,气球的变化是_____。
(方法感悟)在化学实验中,可通过验证反应后生成物的存在,来验证某化学反应的发生。
【答案】Na2SO4和H2SO4 黑色固体逐渐溶解,溶液由无色变为蓝色 酸性和中性溶液都不能使无色酚酞溶液变红(合理即可) Na2SO4和H2SO4都能与BaCl2溶液反应生成白色沉淀 小灯泡先逐渐变暗至熄灭,再逐渐变亮 H2SO4+Ba(OH)2=BaSO4↓+2H2O 先变大后变小直到恢复原状(合理即可)
【解析】
【提出猜想】反应后的溶液中可能酸过量,也可能碱过量,还可能是酸碱恰好完全反应,所以猜想三是Na2SO4和H2SO4.【实验探究】根据实验结论“猜想三正确”,可知溶液中含有H2SO4,加入的CuO能与H2SO4反应生成蓝色的CuSO4溶液。【方案评价】①由于酸性和中性溶液都不能使无色酚酞溶液变色,无法判断溶质成分;②Na2SO4和H2SO4都能与BaCl2溶液反应产生白色沉淀,故该方案也不合理。【学科渗透】向稀H2SO4中逐渐加入Ba(OH)2溶液,反应生成BaSO4白色沉淀和水,溶液中所含能导电的离子的浓度逐渐减小,小灯泡的亮度变暗;当H2SO4和Ba(OH)2恰好完全反应时,烧杯内的水中不含能导电的离子,此时小灯泡熄灭;继续加入Ba(OH)2溶液后,溶液中含有Ba2+和OH-,小灯泡又逐渐变亮。【反思应用】先向瓶内加入氢氧化钠溶液,氢氧化钠溶液能和二氧化碳反应生成碳酸钠,导致瓶内压强减小,在外界大气压的作用下,气球逐渐胀大;然后向瓶内加入盐酸,盐酸与碳酸钠溶液反应放出二氧化碳,又能使瓶内压强恢复到初始状态,该过程中能看到气球逐渐变小直到恢复原状。

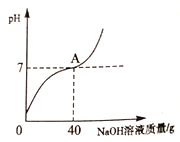
【题目】(2017唐山路南区一模)某学习小组取某地石灰石样品25 g进行测定实验,现将200 g稀盐酸分五次加入石灰石样品中(杂质不溶于水也不参与反应),实验过程所得数据如下表:
次数 | 1 | 2 | 3 | 4 | 5 |
加入稀盐酸的质量/g | 40 | 40 | 40 | 40 | 40 |
生成气体的总质量/g | 2.2 | m | 6.6 | 8.8 | 8.8 |
请计算:
(1)m的值为________g。
(2)25 g石灰石样品中碳酸钙的质量。
(3)反应完全后最终溶液中氯化钙的质量分数。(结果精确到0.1%)
【题目】(2018石家庄长安区质检)某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2),该小组同学进行如下研究。

探究一:该气体的成分
(猜想与假设)小王说:该气体可能是CO2、O2、CO、H2、N2。
小李说:不可能含有CO和H2,因为从药品安全角度考虑,CO有毒,H2________________。
小张说:不可能含有N2,因为___________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
(进行实验)
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(得出结论)
(1)由实验①可知,该气体中肯定含有________,写出该反应的化学方程式________。
(2)由实验②不能确定该气体中不含氧气,理由是_____________。
若要证明含有氧气,请你帮助设计实验_____________。
探究二:维C泡腾片溶液的酸碱性
(3)向维C泡腾片溶液中滴加石蕊溶液,溶液变红,说明溶液显________性。
【题目】我国发行的第五套人民币中,铸造1元、5角和1角硬币的主要材料含有铁、镍(Ni)、铜等。

(查阅资料)氯化镍溶液为绿色。
(猜想假设)根据所学知识,猜想三种金属在金属活动性顺序中的相对位置关系:
猜想一:Fe>Cu>Ni 猜想二:Ni>Fe>Cu猜想三: ____
(实验探究)兴趣小组的同学设计了以下两种方案来进行探究,都得出了相同的实验结论。
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | (1)把一根光亮的铁丝放入盛有NiCl2溶液的试管中 | 铁丝表面有固体析出 | |
(2)把一根镍丝插入盛有CuCl2溶液的试管中 | 镍丝表面有___析出 | ||
方案二 | 分别取三支试管,向其中加入等质量、等浓度的稀盐酸,然后将铁、镍、铜三种金属丝分别插入三支试管中 | ____,加入铁丝、镍丝的试管中溶液变为浅绿色 | 猜想__成立。铁丝与稀盐酸反应的化学方程式为_____ |
(分析讨论)将铁丝打磨光亮的目的是______。
(反思交流)在NiCl2和CuCl2的混合溶液中加入一定量的铁粉,充分反应后过滤得到滤渣,向滤渣中加入足量稀盐酸,有气泡产生,则滤渣中一定含有的物质是__(填化学式)。