题目内容
【题目】在实验室里小红和小英同学合作制取氢气,并对其性质进行探究。
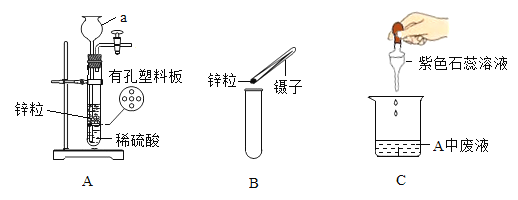
(1)仪器a的名称是_______。
(2)用A装置制取氢气的优点是_______,发生反应的化学方程式是________。
(3)小红向试管中装入锌粒的操作如B所示,其操作的错误是________。
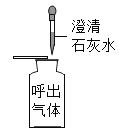
(4)反应后将试管中的物质倒入烧杯中,如C所示,滴加紫色石蕊溶液,紫色石蕊溶液变红色,C中的阳离子是___________。
【答案】长颈漏斗 可随时控制反应的发生或停止 Zn+H2SO4=ZnSO4+H2↑ 将固体投入试管中 Zn2+、H+
【解析】
(1)仪器a的名称是长颈漏斗。
(2)关闭装置A装置中的活塞,氢气不能排出,试管内压强变大,稀硫酸被压进长颈漏斗中与锌粒脱离,反应停止,打开活塞,氢气排出,试管内压强变小,稀硫酸进入试管内与锌粒体接触,反应发生,故用A装置制取氢气的优点是可随时控制反应的发生或停止,发生反应的化学方程式是:Zn+H2SO4=ZnSO4+H2↑。
(3)向试管中装入锌粒的操作:应先将试管横放,将固体放在试管口,再将试管慢慢竖立起来,错误的操作是将固体投入试管中。
(4)反应后将试管中的物质倒入烧杯中,如C所示,滴加紫色石蕊溶液,紫色石蕊溶液变红色,说明溶液显酸性,即反应中稀硫酸是过量的。C中的阳离子是生成的锌离子及过量的氢离子,故填:Zn2+、H+。

 习题精选系列答案
习题精选系列答案【题目】探究二、研究二氧化碳的制取

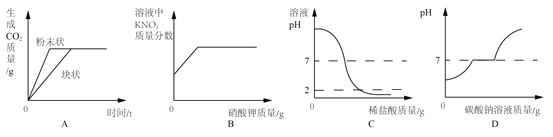
(1)同学们按表进行实验,取等质量的石灰石分别加入两种不同的酸(杂质不与酸反应)进行三次实验,产生二氧化碳体积随时间变化曲线如图1所示。
实验编号 | 药品 |
Ⅰ | 块状大理石、10%稀硫酸溶液 |
Ⅱ | 块状大理石、7%稀盐酸溶液 |
Ⅲ | 大理石粉末、7%稀盐酸溶液 |
①图中丙曲线对应实验_____(选填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
②小组同学讨论确定用图中乙曲线对应的药品制备二氧化碳,反应方程式为_____。
③不用图1中甲曲线对应的药品,理由是_____。
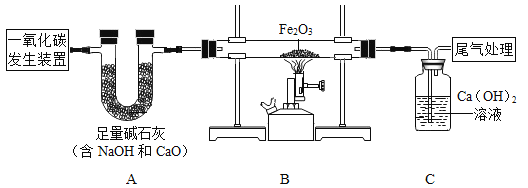
(2)在实验室同学们选用图2装置制取比较纯净、干燥的CO2。
①B装置中发生反应的化学方程式为_____;
②C装置中浓硫酸的作用是_____;
③请在D中简要补画出CO2的收集装置图。_____
(3)取12.5g石灰石于装置A中,向其中加入100g足量的稀盐酸,充分反应后(杂质不参加反应)的质量为108.1g,请计算:
①反应生成二氧化碳气体的质量为_____g;
②充分反应后,A装置内的混合物中含有氯化钙的质量为_____g;
③该石灰石中碳酸钙的质量分数为_____。
(4)反应后所得溶液中的溶质成分是什么?
猜想一:CaCl2; 猜想二:CaCl2和HCl。
①可选择下列物质中的_____(填字母)进行验证。
A 镁条 B 铜片 C 酚酞试液 D 硫酸溶液 E 硝酸银溶液 F 碳酸钙粉末
②实验后确认猜想二正确。取适量上述反应后所得滤液,逐滴滴入碳酸钠溶液,并用pH传感器连续监测,得到如图3曲线(纵坐标为pH,横坐标为时间):据图分析,写出BC段内发生的化学反应方程式为_____;图中CD段上升的原因是_____。