题目内容
【题目】图所示实验中得出的结论正确的是
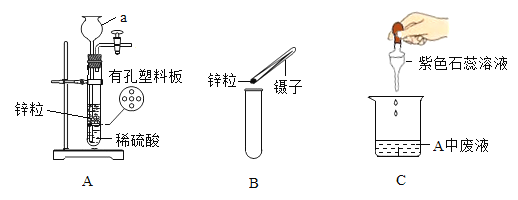
A. 试管中有气泡产生,说明该固体一定是金属
试管中有气泡产生,说明该固体一定是金属
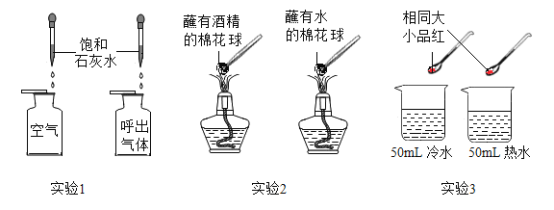
B.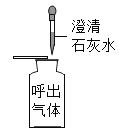 澄清石灰水变浑浊,说明呼出气体中CO2含量大于空气中CO2的含量
澄清石灰水变浑浊,说明呼出气体中CO2含量大于空气中CO2的含量
C.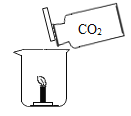 向有一支燃着蜡烛的烧杯中倾倒CO2, 蜡烛熄灭,说明CO2密度大于空气
向有一支燃着蜡烛的烧杯中倾倒CO2, 蜡烛熄灭,说明CO2密度大于空气
D.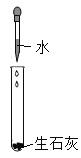 向盛有生石灰的试管中加水,试管外壁发热,说明生石灰溶于水放出热量
向盛有生石灰的试管中加水,试管外壁发热,说明生石灰溶于水放出热量
【答案】C
【解析】
A、向固体滴加盐酸产生气体,不一定是金属,也可能是碳酸盐,故选项错误;
B、向呼出气体中滴入澄清的石灰水,澄清石灰水变浑浊,不能说明呼出气体中CO2含量大于空气中CO2的含量,还需进行对比试验,若同时将澄清石灰水滴入空气中,澄清石灰水不变浑浊,才能证明呼出气体中CO2含量大于空气中CO2的含量,故选项错误;
C、向有一支燃着蜡烛的烧杯中倾倒CO2,蜡烛熄灭,说明CO2密度大于空气,故选项正确;
D、向盛有生石灰的试管中加水,试管外壁发热,不一定说明生石灰溶于水放出热量,可能是生石灰与水发生了反应,放出了热量,故选项错误。故选C。

 名校通行证有效作业系列答案
名校通行证有效作业系列答案【题目】某实验小组为探究酸的化学性质,由甲、乙、丙同学设计并完成了如图所示的实验。
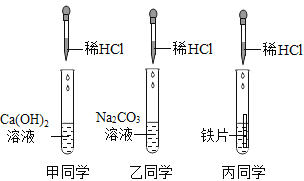
(1)甲同学实验中所发生反应的化学方程式为______________。丙同学实验试管中的反应现象为______________。
[在阅资料] CaCl2、NaCl 的溶液是中性,Na2CO3溶液显碱性。
[实验报究一 ]确定甲、乙同学上述实验后所得溶液中的溶质。
(2)取甲所得溶液少许,加入石蕊试液,溶液显红色,甲所得溶液中一定含有的溶质是_____________(写化学式)
(3)取乙所得溶液少许,加入酚酞试液,溶液显红色,乙所得溶液中一定含有的溶质是______________。(写化学式)
[实验探究二]确定甲、乙同学上述实验所得溶液混合后的成分。
(4)甲、乙同学把上述实验所得溶液倒入同一废液缸中,观察到先有气泡产生,后有白色沉淀生成。同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究。
甲同学猜想: NaCl;
乙同学猜想:NaC1、CaCl2;
丙同学猜想: NaCl、CaCl2、HCl;
你的猜想:______________。
[交流讨论]
(5)你认为_____________同学的猜想一 定不正确, 理由是______________。
[设计实验]请设计实验证明你的猜 想正确。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,向其中滴加_____________。 | ______________。 | 猜想成立。 |
【题目】实验室现有硫酸镁和硫酸钠的固体混合物样品,小明同学想测定样品中硫酸镁的质量分数,先称取该混合物样品20g,完全溶于100g水中。然后取用了一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
次数 | 1 | 2 | 3 | 4 |
加入氢氧化钠溶液的质量/g | 25 | 25 | 25 | 25 |
生成沉淀的质量/g | 2.9 | X | 8.7 | 8.7 |
(1)上表中X的数值为______;原固体混合物样品中硫酸镁的质量分数是 ;
(2)求恰好完全反应时,溶液中溶质的质量分数。(结果精确到0.1%)
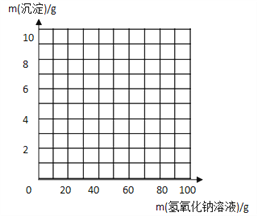
(3)请在下图中画出在20 g 样品中加氢氧化钠溶液的质量与产生沉淀质量变化关系的示意图。
(4)若用氢氧化钡溶液代替氢氧化钠溶液来测定样品中硫酸镁的质量分数,是否可行?并说明理由。