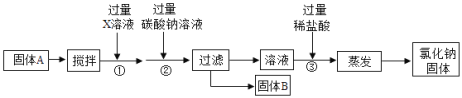
��Ŀ����
����Ŀ��Ϊ̽�������Ļ�ѧ���ʣ�ij��ѧ̽��С���������ʵ����
��������⣩������ʲô��ѧ���ʣ�
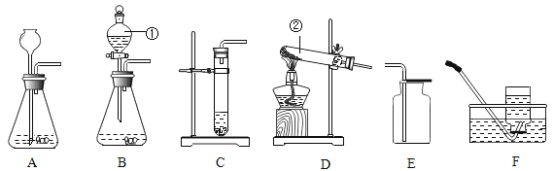
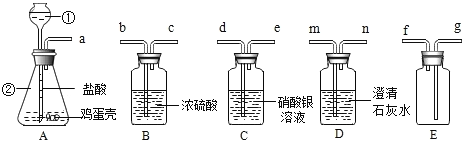
��ʵ��̽����ʯ������˼�ֱ���һƬδ��ĥ����Ƭ�ʹ�ĥ������Ƭ����ʵ��A��B��ʵ��B�й۲쵽��������___���ó�����ϡ���ᷴӦ��������Ľ��ۣ�
����˼�����ۣ�������ʯ����Ϊ����ϡ���ᷴӦ���������壬������ʯ����ʵ��ͽ���___������˼����ʯ�����Թ��м����μ����������ᣬһ�����۲쵽��B����ͬ�����ݴ�ʯ���Ʋ�������е�һ����ѧ���ʣ�
��ʵ��̽���������������ͼCʵ��û�й۲쵽���������Ƿ����˻�ѧ��Ӧ�أ����˺�����˳��Ĺ��壬���ֹ����������ӣ�������˼��ʵ����ۣ��������˳������м�������ϡ���ᣬ����������֪�����в���___������___���ݴ˿�֪C�з�����Ӧ�Ļ�ѧ����ʽΪ___�������ֵó�һ�������еĻ�ѧ���ʣ�
�����������⣩ͬѧ���ֶ�a��b�����ʵijɷֲ�����Ȥ��
��ʵ��̽�����ݶ����ʳɷֵIJ��룬���ʵ��̽�����̽���ɹ���ʯ��ȡ����a��b��Ʒͨ����ϵķ�������a��b�����ʵijɷ֣�
����������ۣ������ʯ����ʵ��������ɣ�����Ϊͨ��ʵ��D�����Ʋ�b�����ʵijɷ֣�ȴ��ȷ��a�����ʵijɷ֣����������Ǹ��������ʵ����ʵ�����Ʋ��b�����ʺ��е�������___(�����ӷ���)����ȷ��a�����ʵijɷ�����Ϊ___��
��ʵ������ۣ�����˼����Ϊȷ��a�����ʣ�С��ͬѧȡ����a��Ʒ������___(�����)�۲쵽������������ȷ����a�����ʵijɷ֣�
���������ܽᣩͨ������ʵ������ܽ������̽�����ʵ�����ʱ������Ҫ�ų�___����̽���������ʿ��ܲ������ţ�
���𰸡���Ƭ����ֱ����ʧ���������� ����ȷ��δ��ĥ����Ƭ������һ����������������ϡ������Ժ���������Ӧ �� �� Al+3AgNO3��Al(NO3)3+3Ag Ag+��Al3+��NO3�� a��b��Ϻ������ɫ��������b�е������Ӻ�a�е������ӽ�����ɵ��Ȼ�������ȷ���Ƿ���ϡ���� ������ͭ ������������
��������
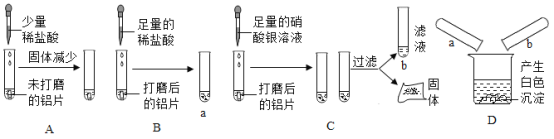
[ʵ��̽����]ʵ��B�й۲쵽����������Ƭ����ֱ����ʧ���������ݣ��ó�����ϡ���ᷴӦ��������Ľ��ۣ�
�����Ƭ����ֱ����ʧ���������ݣ�
[��˼������]
��Ϊδ��ĥ����Ƭ������һ����������������ϡ������Ժ���������Ӧ�������ܺ�����Ӧ�����ʯ����ʵ��ͽ��۲���ȷ��
�������ȷ��δ��ĥ����Ƭ������һ����������������ϡ������Ժ���������Ӧ��
[ʵ��̽����]
�������˳������м�������ϡ���ᣬ����������֪�����в����������������ݴ˿�֪C��������������Ӧ����������������������Ӧ�Ļ�ѧ����ʽΪ��Al+3AgNO3��Al(NO3)3+3Ag��
�����������Al+3AgNO3��Al(NO3)3+3Ag��
[���������]
���������ʵ����ʵ��֪��a��b��ϲ���������˵��b�к��������ӣ�������Ʋ��b�����ʺ��е�������Ag+��Al3+��NO3������ȷ��a�����ʵijɷ�����Ϊ��a��b��Ϻ������ɫ��������b�е������Ӻ�a�е������ӽ�����ɵ��Ȼ�������ȷ���Ƿ���ϡ���ᣮ
���Ag+��Al3+��NO3����a��b��Ϻ������ɫ��������b�е������Ӻ�a�е������ӽ�����ɵ��Ȼ�������ȷ���Ƿ���ϡ���ᣮ
[ʵ�������]
����˼����Ϊȷ��a�����ʣ�С��ͬѧȡ����a��Ʒ������������ͭ��������Ϊ������ͭ�ܺ�ϡ���ᷴӦ�����Ȼ�ͭ��ˮ���۲쵽������������ȷ����a�����ʵijɷ֣�
���������ͭ��
[�������ܽ�]
ͨ������ʵ������ܽ������̽�����ʵ�����ʱ������Ҫ�ų������������ʣ���̽���������ʿ��ܲ������ţ�
��������������ʣ�

 ��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�
��˼ά������ҵ���ټ��ִ�ѧ������ϵ�д�����Ŀ���á����ᡪ������������BaCl2��ų��ж�����H2S(��ˮ��Һ������)������NaOH����H2S��ȡNa2S���д������±�ΪH2S���չ��յĸ��������ɱ�:
�� H2S���չ��յĸ��������ɱ�
��Ŀ | ����(Ԫ/��) |
NaOH | 2500 |
Na2S | 5000 |
��������(�Դ���1��H2S��) | 1114 |
(1)��ҵ����β���迼�Ǿ���Ч������Ч�棬�����������Ϸ��������Ӿ���Ч�濼�����ִ���H2S�ķ�����______(ѡ�ӯ��������)�ġ�
(2)��ij������ÿ��Ҫ����10��H2S��������NaOH���ٶ�__________?(д��������̣��������1λС��)