题目内容
【题目】105.4g稀盐酸跟一定量含少量杂质的石灰石恰好完全反应(杂质不溶解,也不参与反应),生成4.4g二氧化碳。反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑
试求:(要写出计算过程)
(1)石灰石中碳酸钙的质量______;
(2)反应后所得溶液溶质的质量分数_______;
【答案】10g 10%
【解析】
由二氧化碳的质量根据碳酸钙与稀盐酸反应的化学方程式可以计算出发生反应的碳酸钙的质量和生成氯化钙的质量,计算出所得溶液中溶质的质量分数。
解:设石灰石中碳酸钙的质量为x,生成氯化钙的质量为y,
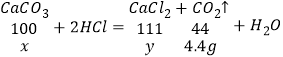
![]() x=10g,
x=10g,
![]() y=11.1g,
y=11.1g,
所得溶液溶质的质量分数为:![]() ×100%=10%;
×100%=10%;
答:(1)石灰石中碳酸钙的质量为10g;
(2)反应后所得的溶液中溶质的质量分数为10%。

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目