题目内容
【题目】某种氯化钠固体中含有少量氯化钙和硫酸镁杂质,现通过下列方法除去杂质:
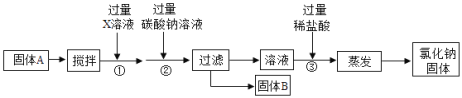
(1)写出X溶液中溶质的化学式________.
(2)写出②处发生的化学反应方程式(写一个即可)________.
(3)在③处加入过量稀盐酸的目的是___?蒸发加入了过量的稀盐酸,为什么蒸发后能得到纯净的氯化钠固体__________?
【答案】Ba(OH)2 Na2CO3+CaCl2=CaCO3↓+2NaCl或Na2CO3+Ba(OH)2=BaCO3↓+2NaOH 除去过量的Na2CO3和反应后生成的NaOH 盐酸易挥发,在蒸发过程中气体逸散到空气中
【解析】
(1)除去少量氯化钙和硫酸镁,应先用足量的氢氧化钡溶液除去硫酸镁,然后用足量的碳酸钠溶液除去氯化钙和过量的氢氧化钡,因此X溶液中溶质是氢氧化钡;
(2)②处发生的反应有:碳酸钠和氯化钙反应生成碳酸钙和氯化钠、碳酸钠与氢氧化钡反应生成碳酸钡和氢氧化钠;
(3)在③处加入过量稀盐酸的目的是除去过量的Na2CO3和反应后生成的NaOH;盐酸易挥发,在蒸发过程中气体逸散到空气中,因此蒸发后能得到纯净的氯化钠固体。

【题目】火锅是我国独创的美食,历史悠久。火锅常用的一种燃料是固体酒精。某化学兴趣小组的同学对“固体酒精”产生了好奇,对其成分进行探究。请你回答下列问题。
(查阅资料)(1)、固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成。
(2)、氯化钙溶液和酒精溶液均呈中性。
(提出问题)固体酒精中的氢氧化钠是否变质?
(实验探究)
(1)、取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现烧杯底部有白色沉淀,请用化学方程式表示该沉淀是如何形成的_____,由此说明氢氧化钠已变质。
(2)、为进一步确定氢氧化钠的变质程度,分组进行探究。
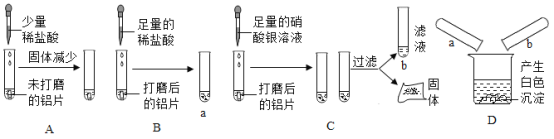
甲组同学取烧杯上层清液于两支试管中,按如图所示进行实验。
实验方案 |
|
|
实验现象 | 溶液变红 | 产生_____ |
实验结论 | 清液中有氢氧化钠 | 清液中有碳酸钠 |
乙组同学认为甲组实验不能证明清液中一定有氢氧化钠,理由是_____。
他们另取烧杯中上层清液,加足量氯化钙溶液,充分反应后,静置,取上层清液,滴加酚酞溶液,酚酞溶液变红。
(反思交流)(1)、乙组实验中加足量氯化钙溶液的目的是_____。
(2)、乙组实验中能否用澄清石灰水代替氯化钙溶液_____(填“能”或“不能”)。
【题目】空气是宝贵的然资源。
下表是空气,如图是以空气、煤等为原料合成尿素(化学式;CO(NH2)2)的流程(部分产物已略去)。请按要求回答相关问题:
空气组成 | N | R | Q | CO | 其它 |
体积分数 | 78% | 21% | 0.93% | 0.034% | 0.02% |
(1)上表中R的名称是_____;
(2)物质X和H2合成氨气的化学方程式是_____;该反应属于_____反应(填基本反应类型)。
(3)分离空气的常用方法有以下两种。
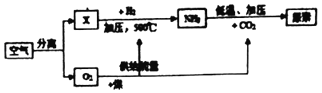
Ⅰ.将空气液化后再气化,液态空气气化时首先分离出氮气。则比较二者的沸点:N2_____O2(选填“高于”“等于”或“低于”)。
Ⅱ.用分子筛分离。分子筛是一种内部分布有均匀微小孔径的固体,通过特制的分了筛把空气中的氧分子吸入孔穴而与其它分子分离,则分子大小;N2_____O2(选填“大于”“等于”或“小于”)。