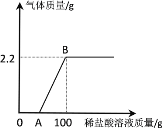��Ŀ����
����Ŀ��ij��ѧ��ȤС���ڹ����ᡢ��λ�ѧ����ʱ��������Щʵ�����۲쵽����������Ҫ���иĽ������ʵ����֤��
����ȤС��С��ͬѧ������ᡢ���к�û���������������������ʵ�飺
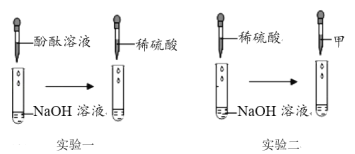
��1��ʵ��һ����NaOH��Һ���ȵ��뼸�η�̪��Һ�����ٵ���ϡ���ᣬ�۲쵽��Һ��____ɫ��Ϊ��ɫ��˵��������ܷ�����Ӧ���������Թ�������ε������NaOH��Һ������������۲쵽____________________________��֤���˵μӵ�ϡ���������
��2�����ա�֤����Ӧ��NaOH��ʧ�ˡ�����Ƕȣ���ͬѧ�������ʵ�������������ϡ�������NaOH��Һ���ٵ������Һ��ͬ��֤������ͼ��ܷ�����Ӧ������Һ������________��ָʾ�����⣩��
��3������ͬѧ�����Ĺ۵�������ɣ������������ᡢ���кͷ�Ӧ��û��������������ϡ������___________��Ӧ�Ϳɹ۲쵽���Ե�����
����ȤС��С��ͬѧ�����CO2ͨ��NaOH��Һ��Ҳ�����������������ʵ��������̽����
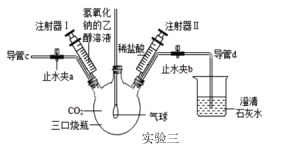
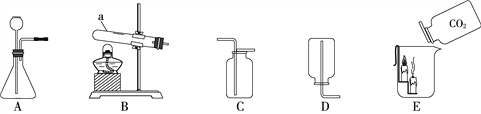
��װ�������Ӻã����������ã�ֹˮ��a��b�ѹرգ�������������ȥ��
[��������]
��CO2���Ҵ�����Ӧ����ʵ��������CO2���Ҵ��е��ܽ���Բ��ơ�
�ڳ�����NaOH�������Ҵ���Na2CO3�����Ҵ���
��4����ע���������������Ƶ��Ҵ���Һע�����CO2��������ƿ�У��������۲쵽��������_________________��д���÷�Ӧ�Ļ�ѧ����ʽ_______________________________________��
��5���ѵ���d�Ƴ�ʯ��ˮ����ֹˮ��a��b���ٴӵ���c����������ƿ�й���N2��Ŀ����_________________________������һ��ʱ����Ȱѵ���d�������ʯ��ˮ�У����Źر�ֹˮ��a���ٰ�ע�������е�ϡ����ע��������ƿ�ڣ��۲쵽������ƿ�в������ݣ�_____________����������Ƕ���֤��CO2��NaOH��Һ�����˷�Ӧ��
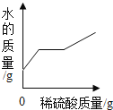
������ʦ��ָ���£�����ȤС�������ͬѧ������CO2����ͨ��һ��Ũ��һ������NaOH��Һ�У������ֻ�ʵ�鼼���ƶ���Ӧ��������Һ��pH���¶ȱ仯�������ͼ1��ͼ2��ʾ��

[��������] ��ʵ�������£�Na2CO3��Һ��NaHCO3��Һ��pH�ֱ�ԼΪ11.0��8.5��
��6��ͼ1�У�BC�η�����Ӧ�Ļ�ѧ����ʽΪ__________________________________________��ͼ2�У�DE���¶ȱ仯��ԭ����________________________________________________��
[��˼����]
��7����������������ķ�Ӧ��С��ͬѧһ����Ϊ����ͨ����Ӧ��ļ��ٻ�������������Լ�_________�仯�ȽǶ���֤��Ӧ�ķ�����������ͨ���ִ������ֶν������ݲⶨ��ʵ�ַ�Ӧ���̵ġ����ӻ�����
���𰸡��� ��һ�������Һ�ű�ɺ�ɫ ����ͭ �������� ���ɰ�ɫ������������� 2NaOH+CO2=Na2CO3 +H2O �ų�װ���ڵĶ�����̼ �ձ��еij���ʯ��ˮ����� Na2CO3+CO2+H2O=2NaHCO3 ������̼������������Һ��Ӧ�ų����� ����
��������
��1��NaOH��Һ�Լ��ԣ���̪��Һ��������Һ��졢�����Ի�������Һ����ɫ����NaOH��Һ���ȵ��뼸�η�̪��Һ�����ٵ���ϡ���ᣬ�۲쵽��Һ�ɺ�ɫ��Ϊ��ɫ��˵��������ܷ�����Ӧ���������Թ�������ε������NaOH��Һ������������۲쵽һ��ʱ�����Һ�ű�ɺ�ɫ��֤���μӵ�ϡ���������
��2��������֤����Ӧ��NaOH��ʧ��������Ƕȣ���ͬѧ�������ʵ�������������ϡ�������NaOH��Һ������Ӧ��2NaOH+H2SO4=Na2SO4+2H2O ���ٵ�������ͭ�����Ȼ�þ���Ȼ����ȣ���Һ��û�в�����ɫ������ͭ��������ɫ������þ���������ɫ����������������ͬ��֤������ͼ��ܷ�����Ӧ���ʼ���Һ����������ͭ��
��3������ͬѧ�����Ĺ۵�������ɣ������������ᡢ���кͷ�Ӧ��û��������������ϡ����������������Һ��Ӧ�Ϳɹ۲쵽������ɫ�������Ե�����
��4����ע���������������Ƶ��Ҵ���Һע�����CO2��������ƿ�У�������������̼���������Ʒ�Ӧ����̼���ƺ�ˮ��װ����ѹǿ��С��������̼�����ھƾ����ܣ��ʹ۲쵽�������Dz�����ɫ������������÷�Ӧ�Ļ�ѧ����ʽΪ��2NaOH +CO2=Na2CO3 +H2O��
��5���ѵ���d�Ƴ�ʯ��ˮ����ֹˮ��a��b���ٴӵ���c����������ƿ�й���N2��Ŀ�����ų�װ���ڵĶ�����̼������һ��ʱ����Ȱѵ���d�������ʯ��ˮ�У����Źر�ֹˮ��a���ٰ�ע�������е�ϡ����ע��������ƿ�ڣ��۲쵽������ƿ�в������ݣ�����ʯ��ˮ����ǣ���������Ƕ���֤��CO2��NaOH��Һ�����˷�Ӧ��
��6����֪��Na2CO3��Һ��NaHCO3��Һ��pH�ֱ�ԼΪ11.0��8.5��ͼ1�У�BC��pH��11��С��8.5�����Է�������̼���ƺͶ�����̼��ˮ��Ӧ����̼�����Ƶķ�Ӧ����ѧ����ʽΪ��Na2CO3+CO2+H2O=2NaHCO3��ͼ2�У�DE���¶ȱ仯��ԭ���Ƕ�����̼������������Һ��Ӧ�ų�������
��7����������������ķ�Ӧ��С��ͬѧһ����Ϊ����ͨ����Ӧ��ļ��ٻ�������������Լ������仯�ȽǶ���֤��Ӧ�ķ�����������ͨ���ִ������ֶν������ݲⶨ��ʵ�ַ�Ӧ���̵������ӻ�����

 ������״Ԫ���Ծ�ϵ�д�
������״Ԫ���Ծ�ϵ�д�