题目内容
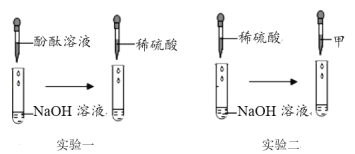
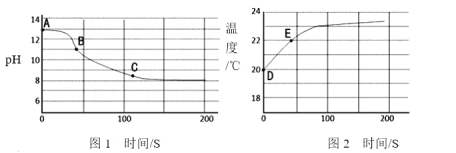
【题目】观察下列各图,回答有关问题。
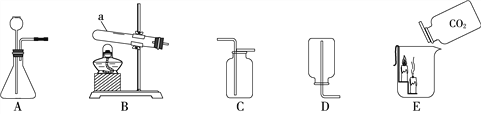
(1)仪器a的名称是______;
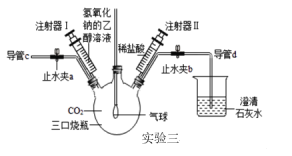
(2)实验室制取CO2,其反应原理可用化学方程式表示为____________,其发生装置可选用上图中的____(选填装置序号,下同),收集装置可选用____;
(3)实验室使用澄清石灰水检验二氧化碳的反应原理可用化学方程式表示为_______________;
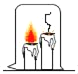
(4)利用收集到的二氧化碳进行图E所示实验,观察到燃着的蜡烛自下而上依次熄灭,体现出二氧化碳的密度比空气大和______的性质。
【答案】试管 CaCO3+2HCl=CaCl2+H2O+CO2↑ A C CO2+ Ca(OH)2== CaCO3↓+ H2O 不可燃不助燃
【解析】
:实验室是用石灰石和稀盐酸来制取二氧化碳的,因此不需要加热;二氧化碳的密度比空气大,能溶于水,因此只能用向上排空气法收集;二氧化碳有三个化学性质:①二氧化碳既不能燃烧也不能支持燃烧,还不能供给呼吸;②与水反应生成碳酸;③能使澄清的石灰水变浑浊。(1)a是试管,是最简单的仪器。(2)实验室是用石灰石和稀盐酸来制取二氧化碳的,因此不需要加热,故选A。碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,二氧化碳的密度比空气大,能溶于水,因此只能用向上排空气法收集。故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;A;C。(3)实验室使用澄清石灰水检验二氧化碳的反应原理可用化学方程式表示为:CO2 + Ca(OH)2 == CaCO3 ↓+ H2O;(4)二氧化碳能够灭火,既证明了一个物理性质,又证明了一个化学性质。体现出二氧化碳的密度比空气大和二氧化碳既不能燃烧也不能支持燃烧。

【题目】罗筝依同学为探究Cu、Al、Ag的金属活动性顺序,做了如下两个实验。请分析实验,完成填空。

(1)试管②中发生了化学反应,现象明显,该反应的化学方程式是_____。
(2)通过实验探究,Cu、Al、Ag三种金属活动性由强到弱的顺序是_____。
(3)两支试管中的反应一段时间后,分别过滤,把滤液倒在烧杯中得到一种蓝色的混合液。黄一格同学由此认为试管①中Cu(NO)3溶液没有反应完,你认为他的结论正确吗?理由是_____。
同学们还想对混合液中的溶质成份进行探究:
(提出猜想)猜想一:_____;
猜想二:_____。
(设计实验)请选择其中一种猜想,并设计实验证明:
实验操作 | 实验现象 | 实验结果 |
取少量溶液于试管中,加入_____溶液 | _____。 | 猜想_____成立 |