题目内容
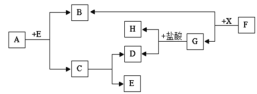
【题目】炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如图。
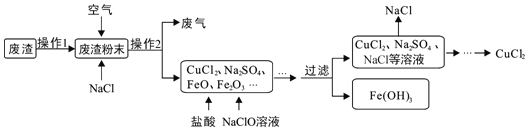
(1)废气中污染空气的气体主要是_____。
(2)在高温条件下,通入空气,CuS、NaCl等物质反应生成CuCl2和Na2SO4,该反应的化学方程式为_____。
(3)(查阅资料)不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH范围的方法,使某种金属氢氧化物沉淀,结合过滤等操作,进行物质分离。下表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH。
Fe(OH)3 | Cu(OH)2 | |
开始沉淀的pH | 1.9 | 4.2 |
沉淀完全的pH | 3.2 | 6.7 |
为了只让上述流程溶液中的Fe3+完全转化为Fe(OH)3沉淀而除去,你认为调节溶液的pH到_____(填数值范围)比较合适。
(4)流程图中能循环利用的物质是_____。
(5)本流程中,铁元素的化合价除+3价外还有_____。
【答案】SO2 CuS+2NaCl+2O2 ![]() CuCl2+Na2SO4 3.2~4.2 NaCl 0、+2
CuCl2+Na2SO4 3.2~4.2 NaCl 0、+2
【解析】
解:(1)由物质的变化可知,废气中含有二氧化硫,能污染空气的气体主要是SO2;
(2)在高温条件下,通入空气,CuS、NaCl等物质反应生成CuCl2和Na2SO4,该反应的化学方程式为:CuS+2NaCl+2O2![]() CuCl2+Na2SO4;
CuCl2+Na2SO4;
(3)由表中的数据可知,氢氧化铁完全沉淀时的pH是3.2,氢氧化铜开始沉淀的pH是4.2,所以Fe3+完全转化为Fe(OH)3沉淀而除去,调节溶液的pH到3.2~4.2比较合适;
(4)由物质的变化可知,氯化钠参加了反应,反应后又生成了,是可以循环利用的物质;
(5)由反应中物质的变化可知,本流程中涉及铁的物质有:单质的铁、氧化亚铁和氧化铁,化合价分别是0、+2、+3,所以本流程中,铁元素的化合价除+3价外还有0、+2。

 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案