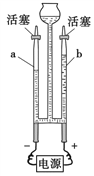
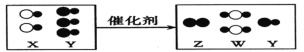
题目内容
【题目】如图为某反应的微观示意图,有关说法正确的是( )
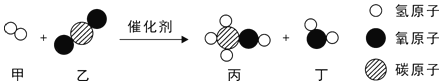
A.该反应属于置换反应
B.该反应不遵守质量守恒定律
C.该反应中甲与丁的分子个数比为3:1
D.丙中氢元素的质量分数最高
【答案】C
【解析】
根据题目信息和质量守恒定律可写出反应的方程式为:二氧化碳和氢气在催化剂作用下反应生成甲醇和水的化学方程式为:CO2+3H2 CH3OH+H2O。
CH3OH+H2O。
A、由上述反应可知,该反应的生成物是两种化合物,不符合置换反应的特点,故A不正确;
B、该反应有新物质生成,属于化学变化,化学变化都遵守质量守恒定律,故B不正确;
C、由方程式可知,该反应中甲与丁的分子个数比为3:1,故C正确;
D、丙中各元素的质量比是:12:(1×4):16=3:1:4,所以氧元素的质量分数最高,故D不正确。
故选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】炼铁产生的废渣中含有大量CuS及少量铁和铁的化合物,工业上以该废渣为原料生产CuCl2的流程图如图。
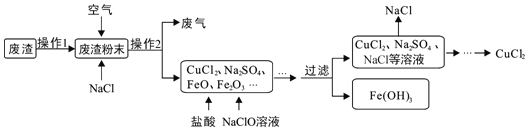
(1)废气中污染空气的气体主要是_____。
(2)在高温条件下,通入空气,CuS、NaCl等物质反应生成CuCl2和Na2SO4,该反应的化学方程式为_____。
(3)(查阅资料)不同金属氢氧化物可以在不同的pH范围内从溶液中沉淀析出,工业上利用调节溶液pH范围的方法,使某种金属氢氧化物沉淀,结合过滤等操作,进行物质分离。下表是氢氧化铁与氢氧化铜开始沉淀与沉淀完全的pH。
Fe(OH)3 | Cu(OH)2 | |
开始沉淀的pH | 1.9 | 4.2 |
沉淀完全的pH | 3.2 | 6.7 |
为了只让上述流程溶液中的Fe3+完全转化为Fe(OH)3沉淀而除去,你认为调节溶液的pH到_____(填数值范围)比较合适。
(4)流程图中能循环利用的物质是_____。
(5)本流程中,铁元素的化合价除+3价外还有_____。
【题目】有一黑色粉末物质可能由氧化铜、木炭、二氧化锰中的两种或三种组成。某兴趣小组对该粉末的成分进行了如下探究和验证。
(提出问题)该黑色粉末含有哪些的成分?
(做出猜想)大家认为黑色粉末的组成共有下面四种可能:
猜想1.木炭和氧化铜;
猜想2.木炭和二氧化锰;
猜想3.______;
猜想4.氧化铜、木炭、二氧化锰。
(查阅资料)①.常温下碳、氧化铜、稀硫酸不与二氧化锰反应;
②.MnO2不能燃烧。
(探究验证)
步骤 | 实验操作 | 实验现象 | 结论 | 理由 |
(1) | 取少量黑色粉末放入试管加入足量的稀硫酸,振荡 | 黑色粉末部分溶解 | 相关反应方程式 ______ | |
(2) | 将(1)反应后的物质过滤、干燥,取一部分滤渣放入横口试管中加强热,并不断鼓入空气 | 有火星产生 | 证明混合物中含有______ | ______ |
(3) | ①将(2)所得另一部分滤渣加5%的过氧化氢溶液 | 有大量能使带火星的木条复燃的气体产生 | 证明混合物中含有______ | |
②向(2)所得滤液中加入5%的过氧化氢溶液 | 有大量能使带火星的木条复燃的气体产生 | ______ |
(结论)上述猜想中正确的是______