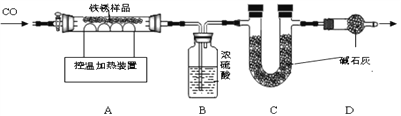
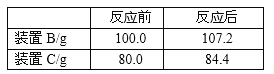
题目内容
【题目】甲、乙两种物质的溶解度曲线如图所示。下列叙述不正确的是
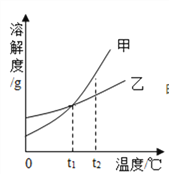
A. t3℃时,将甲的饱和溶液变为不饱和溶液,可采取升温的方法
B. t2℃时,甲和乙的饱和溶液各100 g,其溶质的质量一定相等
C. t1℃时,将甲、乙的饱和溶液各蒸发掉10g水,析出甲的质量大
D. 分别将100 g甲、乙的饱和溶液从t3℃降到t1℃,析出甲的质量大
【答案】C
【解析】A、甲的溶解度随着温度的升高而增大,所以t3℃时,将甲的饱和溶液变为不饱和溶液,可采取升温的方法,故A说法正确;B、t2℃时,甲和乙的溶解度相等,所以相同质量的溶剂中含有相同的溶质,所以t2℃时,甲和乙的饱和溶液各100 g,其溶质的质量一定相等,故B说法正确;C、t1℃时,乙的溶解度大于甲的溶解度,所以10g水中溶解的乙比溶解的甲多,所以t1℃时,将甲、乙的饱和溶液各蒸发掉10g水,析出乙的质量大,故C说法错误;D、从t3℃降到t1℃甲的溶解度减小的幅度比乙溶解度减小的幅度大,所以析出的甲的质量大,故D说法正确。故选C。

练习册系列答案
相关题目
【题目】在一定条件下,一个密闭容器内发生某反应,测得反应过程中各物质的质量部分数据如下表所示.下列未知数据计算正确的是( )
物 质 | a | b | c | d |
反应前的质量/g | 20 | 20 | 0 | 0 |
反应一段时间后的质量/g | 12 | 4 | 6 | ① |
反应后的质量/g | ② | 0 | ③ | ④ |
A. ①为22g B. ②为8g C. ③为12g D. ④为22.5g