��Ŀ����
����Ŀ������������������ͬ�������Ϲ�ϵ���У�
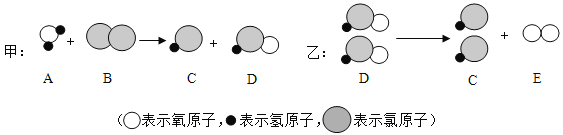
��һ�������Ĺ㷺Ӧ��
��1����������ͨ����Ϊ�����֣����������Ͻ����Ҫ���������_________��д����������ɸ֡��з�����Ӧ�Ļ�ѧ����ʽ_________��
��2��������������;�ˮ������ѧԭ���ǣ�4K2FeO4+10H2O=4X+3O2+8KOH��X�Ļ�ѧʽ��_________ ��
��������������ʴ������
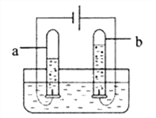
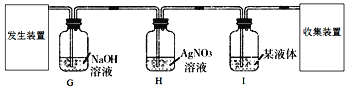
��1���������������Ʒ����������� _________������ţ���
a. ��ʪ������ b. ��������� c. ���ֽ���ʳ��ˮ��
��2���������д�������ת����Fe(OH)2 ![]() Fe(OH)3���÷�Ӧ�Ļ�ѧ����ʽΪ_________��
Fe(OH)3���÷�Ӧ�Ļ�ѧ����ʽΪ_________��
������������ɷ����ⶨ
��1��������һ����Fe2O3nH2O�����ܺ�FeCO3��FeCO3��ϡ����ķ�Ӧ��CaCO3����)������ij������Ʒ�м�ϡ���ᣬ_________��������֤������FeCO3��
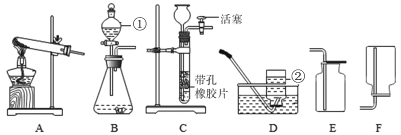
��2����ȡ23.2gֻ��Fe2O3nH2O������������Ʒ������ͼװ��ʵ�飮
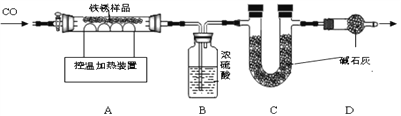
���������ϡ�
��Ũ���������ˮ�ԣ���ʯ��������ˮ�Ͷ�����̼���壮
����110��ʱ��Fe2O3nH2O��ȫ�ֽ�ΪFe2O3��H2O��
��500��ʱFe2O3�ſ�ʼ����ԭ�����¶Ȳ�ͬʱ���������Fe3O4��FeO����ɫ����Fe��
��3����װ���м���������Ʒǰ������еIJ�����________��
��4��ʵ��ʱ����ͨ��CO��Ŀ���� _________ ��
��5�������ȳ���500��ʱ���۲쵽A�е�������_________��
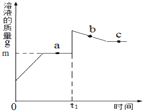
��6���±�Ϊ������700��ʱ�������ݣ���ͼΪA�й��������ͼ����¶ȹ�ϵͼ
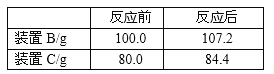

�ش���������
��Fe2O3nH2O��n��ֵΪ_________��ͼ��m��ֵΪ_________��
������װ��D��������n��ֵ_________���ƫ����ƫС�����䡱��
��700������ʱ�����ڹ������Ļ�ѧʽΪ_________��
�ܸ�װ����һ����ȱ�ݣ���θĽ���_________��
���𰸡� ��̼���IJ�ͬ C + O2 ![]() CO2 Fe(OH)3 c 4Fe(OH)2+2H2O+O2 ��4Fe(OH)3 �����ݲ��� ���װ�õ������� ��װ���еĿ�������ֹ����ʱ������ը ����ɫ��ĩ��ɺ�ɫ 4 14.4g ���� FeO ��β������װ��
CO2 Fe(OH)3 c 4Fe(OH)2+2H2O+O2 ��4Fe(OH)3 �����ݲ��� ���װ�õ������� ��װ���еĿ�������ֹ����ʱ������ը ����ɫ��ĩ��ɺ�ɫ 4 14.4g ���� FeO ��β������װ��
����������һ����1�������Ǻ�̼��Ϊ2%��4.3%�����Ͻ𣬸��Ǻ�̼��Ϊ0.03%��2%�����Ͻ���������Ҫ�ɷֶ���������Ҫ�����Ǻ�̼����ͬ�������������ɸ����Ǽ��������еĺ�̼����������Ӧ�Ļ�ѧ����ʽ��C+O2![]() CO2����2�����������غ㶨�ɣ���Ӧǰ��ԭ�ӵ��������Ŀ���䣬��ӦǰKԭ��8����Feԭ��4����Oԭ��26����Hԭ��20������Ӧ��Kԭ��8����Feԭ��0����Oԭ��14����Hԭ��8��������4X�к���4��Feԭ����12��Oԭ����12��Hԭ�ӣ���X�Ļ�ѧʽ��Fe(OH)3����������1��������������������ˮͬʱ���õģ�ʳ��ˮ�ܼӿ�������ʴ�ٶȣ���ѡc����2���������д�������ת����Fe(OH)2
CO2����2�����������غ㶨�ɣ���Ӧǰ��ԭ�ӵ��������Ŀ���䣬��ӦǰKԭ��8����Feԭ��4����Oԭ��26����Hԭ��20������Ӧ��Kԭ��8����Feԭ��0����Oԭ��14����Hԭ��8��������4X�к���4��Feԭ����12��Oԭ����12��Hԭ�ӣ���X�Ļ�ѧʽ��Fe(OH)3����������1��������������������ˮͬʱ���õģ�ʳ��ˮ�ܼӿ�������ʴ�ٶȣ���ѡc����2���������д�������ת����Fe(OH)2 ![]() Fe(OH)3���÷�Ӧ�Ļ�ѧ����ʽΪ��4Fe(OH)2+2H2O+O2 ==4Fe(OH)3��������FeCO3��ϡ����ķ�Ӧ��CaCO3���ƣ�����FeCO3��ϡ������ж�����̼�������ɣ���ij������Ʒ�м�ϡ���ᣬ�����ݲ�����֤������FeCO3����3����װ���м���������Ʒǰ������еIJ����Ǽ��װ�õ������ԣ���4��ʵ��ʱ����ͨ��CO��Ŀ������װ���еĿ�������ֹ����ʱ������ը����5��500��ʱFe2O3�ſ�ʼ����ԭ�������ȳ���500��ʱ������������ԭΪ�����۲쵽A�е������Ǻ���ɫ��ĩ��ɺ�ɫ����6����Ũ���������ˮ�ԣ�B�����ӵ�������Ϊˮ����������ʯ��������ˮ�Ͷ�����̼������ʵ����ˮ�ѱ�Ũ�������գ���Cװ�����ӵ�����Ϊ���ɶ�����̼��������Fe2O3nH2O�У�����
Fe(OH)3���÷�Ӧ�Ļ�ѧ����ʽΪ��4Fe(OH)2+2H2O+O2 ==4Fe(OH)3��������FeCO3��ϡ����ķ�Ӧ��CaCO3���ƣ�����FeCO3��ϡ������ж�����̼�������ɣ���ij������Ʒ�м�ϡ���ᣬ�����ݲ�����֤������FeCO3����3����װ���м���������Ʒǰ������еIJ����Ǽ��װ�õ������ԣ���4��ʵ��ʱ����ͨ��CO��Ŀ������װ���еĿ�������ֹ����ʱ������ը����5��500��ʱFe2O3�ſ�ʼ����ԭ�������ȳ���500��ʱ������������ԭΪ�����۲쵽A�е������Ǻ���ɫ��ĩ��ɺ�ɫ����6����Ũ���������ˮ�ԣ�B�����ӵ�������Ϊˮ����������ʯ��������ˮ�Ͷ�����̼������ʵ����ˮ�ѱ�Ũ�������գ���Cװ�����ӵ�����Ϊ���ɶ�����̼��������Fe2O3nH2O�У�����![]() ��n=4����ϵͼ��m��ֵΪʣ���������������ͷ�Ӧ���ɵ���������֮�ͣ���μӷ�Ӧ��������������Ϊx��������������Ϊy��
��n=4����ϵͼ��m��ֵΪʣ���������������ͷ�Ӧ���ɵ���������֮�ͣ���μӷ�Ӧ��������������Ϊx��������������Ϊy��
Fe2O3+3CO![]() 2Fe+3CO2��
2Fe+3CO2��
160 112 132
![]() y 4.4g
y 4.4g
![]() ��
�� ![]() =5.3g��y=3.7g��ʣ����������Ϊ��23.2g(5.3g+7.2g)+3.7g=14.4g���ڸ��ݢٵķ���������װ��D��������n��ֵ���䣻��700������ʱ�����ڹ������Ļ�ѧʽΪFeO����һ����̼�ж����ǿ�����Ⱦ��ʸ�װ����һ����ȱ�ݣ���θĽ���β������װ�á�
=5.3g��y=3.7g��ʣ����������Ϊ��23.2g(5.3g+7.2g)+3.7g=14.4g���ڸ��ݢٵķ���������װ��D��������n��ֵ���䣻��700������ʱ�����ڹ������Ļ�ѧʽΪFeO����һ����̼�ж����ǿ�����Ⱦ��ʸ�װ����һ����ȱ�ݣ���θĽ���β������װ�á�

 â���̸������Ծ�ϵ�д�
â���̸������Ծ�ϵ�д�