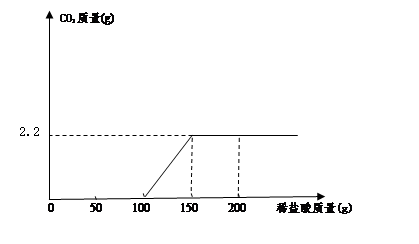题目内容
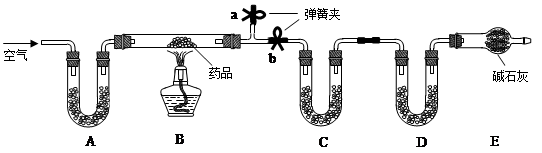
(7分)已知:常温下,CO2、水都能与过氧化钠(化学式 Na2O2)反应产生 O2,其中CO2 与 Na2O2 反应的化学方程式为 2CO2 + 2Na2O2 =2Na2CO3 +O2。某校化学活动小组为探究 CO2与Na2O2反应的产物的性质,设计了如下图所示的实验装置。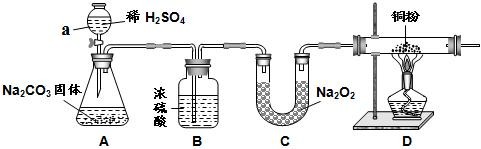
⑴仪器 a 的名称是: 。
⑵装置 B 的作用是 。
⑶装置 A 中,发生反应的化学方程式 。
⑷装置 D 玻璃管中,可以观察到的现象是 ,该反应的化学方程式为 。
⑸反应后,将装置 C 中的固体物质溶于水配成溶液,然后向该溶液中加入 (选填“盐酸”、“CaCl2 溶液”、“石蕊试液”之一),会出现 的现象。
⑹反应完毕后,测得装置 C 的总质量增加了 14g,则产生 O2 的质量为 g。
⑴ 分液漏斗 ⑹ 8
⑵ 除去CO2中的水蒸气(或干燥CO2)
⑶ Na2CO3 + H2SO4 = Na2SO4 + H2O + CO2 ↑
⑷ 红色粉末逐渐变黑 2Cu + O2 △ 2CuO
⑸ 盐酸 / CaCl2溶液/ 石蕊试液 无色气泡 / 白色沉淀 / 溶液变蓝
解析试题分析:(2)浓硫酸具有吸水性,能做干燥剂;
(3)碳酸钠与硫酸反应生成硫酸钠、水和二氧化碳:Na2CO3+ H2SO4 = Na2SO4 + H2O + CO2 ↑;
(4)过氧化钠与二氧化碳反应生成的氧气与铜反应会生成氧化铜,故现象是红色的粉末变成黑色:
2Cu + O2 △ 2CuO;
(5)过氧化钠与二氧化碳反应生成的是氧气和碳酸钠,那么C 中的固体物质是碳酸钠固体,加盐酸会生成二氧化碳气体,加氯化钙会生成碳酸钙沉淀,由于碳酸钠溶液呈碱性,若加紫色石蕊试液石蕊会变成蓝色;
(6)装置 C中发生反应的化学方程式为:2CO2 + 2Na2O2 =2Na2CO3 +O2,装置 C 的总质量增加了 14g,利用差量法,那么生成氧气的质量为8g。
考点:实验探究

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案化学扑克是用卡片类扑克为载体,按照一定规则进行游戏的一种学习方式。请你和大家一起来玩化学扑克吧。
(1)对出规则:甲出一对表示相同物质的牌,其他玩家也必须跟进任何一结表示相同物质的牌。若甲出的牌为:“生石灰”、“CaO”。乙有如下五张牌:“氢氧化钠”、“氢氧化钙”、“火碱”、“NaOH”、“Ca(OH)2”,则乙有种符合对出规则的出牌组合;
(2)单补规则:甲出一张牌作为反应物,乙必须跟出一张能与其反应的牌,当反应物凑齐后,后面的玩家才能跟出该反应的生成物。若甲出的牌为“CaCO3”,乙有如下四张牌:“氧气”、“盐酸”、“ NaOH”、“ CuO”,则乙应跟出的牌为 ;丙有如下四张牌:“CO2”、“CaCl2”、“CO”、“H2O”,丙不能跟出的牌为 ;
(3)串出规则:甲出一个化学方程式,其他玩家也必须跟进一个基本反应类型相同的化学方程式。若甲出“NaOH+HCl=NaCl+H2O”,则乙应出 (填字母)。
| A.NH3+HCl=NH4Cl | B.H2CO3=H2O+ CO2↑ |
| C.H2S+Cl2=" 2HCl" +S↓ | D.KI+AgNO3=KNO3+AgI↓ |
复分解反应的定义可以用字母AB+CD=AD+CB来表示.某化学兴趣小组探究稀盐酸与以下四种物质是否能发生复分解反应:
| NaCl溶液 | K2CO3溶液 | AgNO3溶液 | NaOH溶液 |
(2)甲乙设计了以下三个实验,请你在空白处填写相关内容:
| | 实验操作 | 实验现象 | 实验结论 |
| 实验1 | 在K2CO3溶液中加入稀盐酸 | | 稀盐酸与K2CO3溶液发生了复分解反应 |
| 实验2 | 在AgNO3溶液中加入稀盐酸 | 有白色沉淀生成 | |
| 实验3 | 在NaOH溶液中加入稀盐酸 | 没有明显现象 | 甲乙同学:不发生反应 |
(4)在实验3中,甲乙两同学因为观察到没有明显的实验现象,故判断该反应不能进行,你 (填“同意”或“不同意”)他们的看法,若不同意,请设计实验证明该反应能发生.可用试剂:NaOH溶液、稀盐酸、石蕊试液.
| 实验内容与操作 | 实验现象 | 实验结论 |
| | | |
小军同学在学习酸碱盐有关知识时,对一些沉淀物质的颜色产生了兴趣。老师告诉他氢氧化铜是蓝色、氢氧化铁是红褐色,让他自己探究氢氧化亚铁的颜色。下面请你和他一起探究。
【查阅资料】
(1)铁有两种氢氧化物,它们可以分别由相对应的可溶性盐与碱溶液反应而制得。
(2)氢氧化亚铁在空气中立即被氧化。
(3)硫酸铜溶液是蓝色,硫酸亚铁溶液是浅绿色。
【提出猜想】
氢氧化亚铁是浅绿色。
【实验过程】
在2支试管里分别加入少量FeCl3和FeSO4溶液,然后滴入NaOH溶液,观察现象。请补充完成下表:
| | FeCl3溶液 | FeSO4溶液 |
| 滴入NaOH溶液的现象 | 生成红褐色沉淀 | 先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色沉淀。 |
| 化学方程式 | ① | FeSO4+2NaOH = Fe(OH)2↓+Na2SO4 Fe(OH)2 + ② + H2O = ③ (完成并配平此化学方程式) |
(1)氢氧化亚铁是 ① 色而不是浅绿色。
(2)小军联系到CO2与C的反应,认为FeCl3溶液可以转化为FeCl2溶液。你认为小军的理由是 ① 。
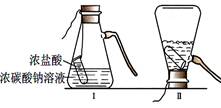
(10分)在学习盐的性质时,某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)
进行反应,有白色沉淀产生,过滤后得到澄清滤液。同学们对该实验进行了一系列的探究。
Ⅰ.定性探究:
探究一:M溶液中的溶质是什么?
(1)【提出猜想】该组同学认为M溶液的溶质有两种可能:
①是 ,
②是CaCl2.
【收集资料】CaCl2水溶液呈中性。
(2)【设计实验】同学们设计了如下方案并进行实验:
| 实验操作 | 实验现象 | 实验结论 |
| 取少量M溶液于试管中,向其中滴加 | | 猜想①正确。碳酸钠与其反应的化学方程式为 |
探究二过滤后澄清滤液中会有哪些溶质?
【提出猜想】猜想一:NaOH 和Na2CO3 ;
猜想二: ;
猜想三:NaOH 。
(3)【实验验证】同学们经过交流讨论,设计以下实验方案确定滤液中溶质的组成:
| 实验操作 | 实验现象 | 实验结论 |
| 分别取少量滤液于A、B两支试管中,A中加入CaCl2溶液, B中加入 溶液 | 若A中产生白色沉淀,B中没有沉淀 | “猜想一”成立 |
| | “猜想二”成立 | |
| | “猜想三”成立 |
Ⅱ.定量探究:
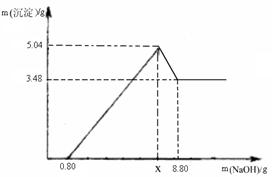
【提出问题】过滤后澄清滤液中NaOH的质量分数是多少?
【设计实验】
小明同学取100g过滤后澄清滤液于烧杯中,向烧杯中逐滴加入过量的稀盐酸,产生的气体与所加入稀盐酸质量关系如下图所示:计算过滤后澄清滤液中NaOH的质量分数是多少?(请列出计算过程)