题目内容
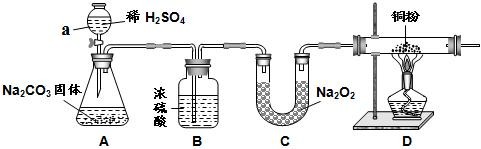
(4分)某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如下图所示实验,并对反应后锥形瓶中残留废液进行探究(不考虑发泡剂等类物质)。
【提出问题】废液中所含溶质是什么物质?
【猜想与假设】
猜想1:废液中的溶质可能是NaCl、Na2CO3和HCl;
猜想2:废液中的溶质只有NaCl;
猜想3:废液中的溶质是NaCl和HCl;
猜想4:废液中的溶质是__________________。
【讨论与交流】小明认为猜想1无需验证就知道是错误的。他的理由是 。
【实验与结论】
(1)为验证猜想2,甲同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是甲认为猜想2正确。甲同学的实验________(填“能”或“不能”)验证猜想2的正确性,原因是________________________________。
(2)乙同学为验证猜想3,选锌粒做试剂。假设猜想3是正确的,验证时反应的化学方程式 。
(3)若猜想4正确,且最终欲得到纯净的氯化钠溶液需加入_____溶液。
【拓展与应用】
若废液中的溶质是NaCl和HCl,根据HCl的性质,无需另加试剂,只要对废液进行_________操作即可从废液中得到NaCl固体。此方法的缺点是_________________。
【猜想与假设】NaCl和Na2CO3 【讨论与交流】 盐酸和Na2CO3不能共存
【实验与结论】(1)不能 甲同学的实验只能证明溶液中含有氯离子,不能确定溶液中只有氯化钠,还可能有盐酸,若有盐酸也会看到相同的实验现象
(2) 2HCl + Zn= ZnCl2 + H2↑ (3)适量CaCl2溶液
【拓展与应用】 蒸发 氯化氢气体排放到空气中引起污染
解析试题分析:【猜想与假设】反应后溶液中溶质的成分:不仅要考虑生成物,还要考虑反应物是否过量,所以猜想4:废液中的溶质是:NaCl和Na2CO3
【讨论与交流】小明认为猜想1无需验证就知道是错误的。他的理由是:盐酸和Na2CO3不能共存,会继续反应
【实验与结论】(1)为验证猜想2,甲同学取少量废液装入试管中,然后滴入AgNO3溶液,产生白色沉淀,滴加稀硝酸沉淀不溶解。于是甲认为猜想2正确。甲同学的实验不能验证猜想2的正确性,原因是甲同学的实验只能证明溶液中含有氯离子,不能确定溶液中只有氯化钠,还可能有盐酸,若有盐酸也会看到相同的实验现象
(2)乙同学为验证猜想3,选锌粒做试剂。假设猜想3是正确的,验证时反应的化学方程式:2HCl + Zn= ZnCl2 + H2↑
(3)若猜想4正确,且最终欲得到纯净的氯化钠溶液,实际就是除去杂质Na2CO3,所以只需加入适量CaCl2溶液
【拓展与应用】若废液中的溶质是NaCl和HCl,根据HCl是气体的性质,无需另加试剂,只要对废液进行蒸发操作即可从废液中得到NaCl固体,此方法的缺点是氯化氢气体排放到空气中引起污染
考点:反应后溶液中溶质的成分探究,盐酸、碳酸钠的化学性质

 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案(6分) 实验室中有一瓶标签受损的无色液体,如图所示。这瓶无色液体是什么呢? 实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸和蒸馏水中的一种。
(1)大家讨论后一致认为不可能是蒸馏水,理由是 。
(2)为确定该液体成分,同学们继续进行了如下实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取该液体适量于试管中,向其中加入少量 粉末。 | 没有气泡产生。 | 该液体不是过氧化氢溶液。 |
| 步骤二:取该液体适量于试管中,向其中滴加少量氯化钡溶液。 | | 该液体是稀硫酸。 |
(1)大家认为标签受损的原因可能是 ;
(2)如果该液体是过氧化氢溶液,则步骤一中产生的变化用化学方程式表示为 。
某化学课堂围绕,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格)。
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的小烧杯中。
【学生板演】该反应的化学方程式 。
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【假设猜想】针对疑问,太家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.不合理的猜想是 。
【实验探究】(1)丙组同学取烧杯中的溶液少量于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有 。
(2)为了验证其余猜想,各学习小组利用烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,进行如下三个方案的探究.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 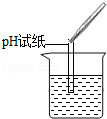 | 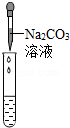 | 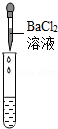 |
| 实验现象 | 试纸变色,对比比色卡,pH<7 | 。 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出【实验探究】(2)中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中的错误是 。
(2)实验方案中也有一个是错误的,错误的原因是 。
实验课上,张影同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
(1)余承骏同学却说:“这种无色溶液中不一定含有氢氧化钠。”他做了如下实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 无色溶液中含有氢氧化钠 |
宋楷认为余承骏的实验方案不严密,不能证实无色溶液中一定含有氢氧化钠,理由是: 。
(2)宋楷设计了另一个实验:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入足量的CaCl2溶液 ②过滤,向滤液中滴加几滴硫酸铜溶液 | ③ ④有蓝色沉淀生成 | 无色溶液中确实含有氢氧化钠 |
(3)宋楷的实验可靠性高的原因是 。