题目内容
复分解反应的定义可以用字母AB+CD=AD+CB来表示.某化学兴趣小组探究稀盐酸与以下四种物质是否能发生复分解反应:
| NaCl溶液 | K2CO3溶液 | AgNO3溶液 | NaOH溶液 |
(2)甲乙设计了以下三个实验,请你在空白处填写相关内容:
| | 实验操作 | 实验现象 | 实验结论 |
| 实验1 | 在K2CO3溶液中加入稀盐酸 | | 稀盐酸与K2CO3溶液发生了复分解反应 |
| 实验2 | 在AgNO3溶液中加入稀盐酸 | 有白色沉淀生成 | |
| 实验3 | 在NaOH溶液中加入稀盐酸 | 没有明显现象 | 甲乙同学:不发生反应 |
(4)在实验3中,甲乙两同学因为观察到没有明显的实验现象,故判断该反应不能进行,你 (填“同意”或“不同意”)他们的看法,若不同意,请设计实验证明该反应能发生.可用试剂:NaOH溶液、稀盐酸、石蕊试液.
| 实验内容与操作 | 实验现象 | 实验结论 |
| | | |
(1)同意(2)
(3)HCl+AgNO3 =HNO3 +AgCl↓(4)不同意 实验操作:向稀盐酸中滴加几滴石蕊试液,再滴加氢氧化钠溶液;实验现象:溶液由红色变成紫色;实验结论:盐酸与氢氧化钠发生了化学反应. 实验操作 实验现象 实验结论 实验1 在K2CO3溶液中加入稀盐酸 有气泡生成 稀盐酸与K2CO3溶液发生了复分解反应 实验2 在AgNO3溶液中加入稀盐酸 有白色沉淀生成 稀盐酸与AgNO3溶液能发生复分解反应 实验3 在NaOH溶液中加入稀盐酸 没有明显现象 甲乙同学:不发生反应
解析

练习册系列答案
 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
某实验小组对实验室制取氢气的反应原理进行探究。
【知识回顾】能产生氢气的化学反应有: ①水电解 ②活泼金属与酸反应
【讨论交流】反应①的化学方程式 ;同学们讨论后认为该反应不适用于实验室制取氢气。
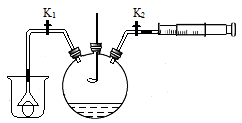
【实验探究】为了探究哪种物质更适合用于实验室制取氢气,大家设计了如下实验: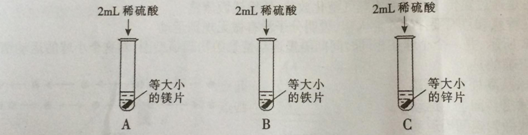
【分析与结论】填写实验报告。
| 实验 | 实验现象 | 实验结论 |
| A | 剧烈反应,迅速产生大量气泡,试管外壁 | 反应速率过快,气体不便收集,不能用于实验室制取氢气 |
| B | 缓慢产生少量气泡 | 反应速率过慢,不能用于实验室制取氢气 |
| C | 较快产生大量气泡,试管外壁发热 | |
【知识拓展】(1)确定实验室制取气体的反应原理时,要考虑诸多因素,如反应的快慢、收集的难易、 等。
(2)用稀盐酸制取氢气时,制得的气体中可能会增加的杂质为 。
同学们运用对比的学习方法探究碱的性质。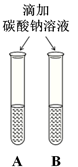

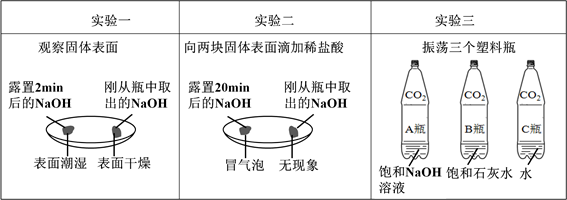
(1)由上图实验一、二可知,氢氧化钠会吸收空气的 ,因此要密封保存。
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C, A瓶内发生反应的化学方程式为 ,对比A瓶与 (选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应。
(3)同学们设计如下两种方案鉴别氢氧化钠溶液与氢氧化钙溶液(分别编号为A、B)。
| 方案一 | 方案二 | 分析 |
| 微热(不考虑水分蒸发) | 两种方案中均观察到A试管内出现白色浑浊,A中试剂为 ; 方案二的设计原理是利用了 。 |
(4)同学们看到盛有NaOH的试剂瓶上标注着“NaOH含量不少于96.0%”,开始如下探究:
【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】工业制取NaOH的反应原理是:2NaCl + 2H2O
 2NaOH + H2↑ + Cl2↑,
2NaOH + H2↑ + Cl2↑,然后蒸发溶剂获得NaOH固体(在化工生产中,原料往往不能完全转化为产品)。
【提出猜想】杂质为碳酸钠和氯化钠。
【实验探究】取样溶于水,并分成两份。
步骤①:向一份溶液中滴加酚酞试剂;
步骤②:向另一份溶液中滴加过量稀硝酸;
步骤③:向②所得溶液中继续滴加硝酸银溶液。
【实验结论】猜想正确。
请分析:
Ⅰ.步骤①中可观察到液体变 色;
Ⅱ.步骤②所得溶液中的溶质除NaCl外,还有 ;
Ⅲ.写出步骤③中发生反应的化学方程式 ;
Ⅳ.上述实验中步骤 (填写序号)是没有必要进行的。