题目内容
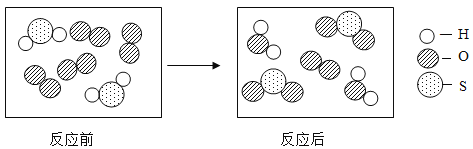
【题目】已知 2.6 g 的某物质在密闭容器内充分燃烧,生成 1.8 g 水、6.6 g 二氧化碳和 1.4 g 一氧化碳,则该物质分子与参加反应氧气分子的个数比为_____;该反应的化学方程式为_____。
【答案】4:9 4C2H2+9O2![]() 6CO2+4H2O+2CO
6CO2+4H2O+2CO
【解析】
已知2.6g的某物质在密闭容器内充分燃烧,生成1.8 g水、6.6g二氧化碳和1.4 g一氧化碳,则参加反应的氧气的质量为1.8g+6.6g+1.4g-2.6g=7.2g,
6.6g二氧化碳中含有碳元素质量为: ![]() ,
,
1.8g水中含氢元素的质量为: ![]() ,
,
1.4g一氧化碳中含有碳元素质量为: ![]() ,
,
碳元素和氢元素的质量之和为1.8g+0.2g+0.6g=2.6g。某物质中只含有碳元素和氢元素,不含氧元素,碳元素和氢原子的个数比为![]() ,设其化学式为CxHx。参加反应的氧气与生成二氧化碳、水和一氧化碳的分子个数为:
,设其化学式为CxHx。参加反应的氧气与生成二氧化碳、水和一氧化碳的分子个数为:![]() ,根据反应前后原子的个数相等,某物质和氧气在点燃的条件下生成二氧化碳、水和一氧化碳,
,根据反应前后原子的个数相等,某物质和氧气在点燃的条件下生成二氧化碳、水和一氧化碳,
设反应的化学方程式为:zCxHx+9O2![]() 6CO2+4H2O+2CO,zx=8,若x=2,z=4,则参加反应的该物质分子与氧气分子的个数比为4:9。该反应的化学方程式为:4C2H2+9O2
6CO2+4H2O+2CO,zx=8,若x=2,z=4,则参加反应的该物质分子与氧气分子的个数比为4:9。该反应的化学方程式为:4C2H2+9O2![]() 6CO2+4H2O+2CO。
6CO2+4H2O+2CO。

 阅读快车系列答案
阅读快车系列答案【题目】某学习小组拟在实验室里利用空气和镁粉为原料制取少量氮化镁(Mg3N2)。查阅资料可知 Mg、Mg3N2能发生如下反应:
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]()
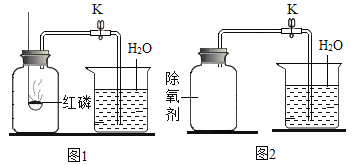
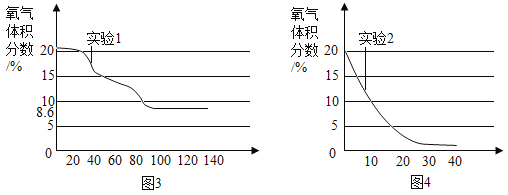
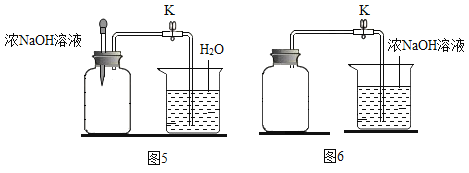
实验中所用的装置和药品如图所示(镁粉、还原铁粉均已干燥,装置内所发生的反应是完全的,整套装置的末端与干燥管相连)。回答下列问题:
(1)连接并检查实验装置的气密性,实验开始时,将空气通入实验装置,则气流流经装置的顺序是_____(填装置序号)。D装置中发生反应的化学方程式为_____。
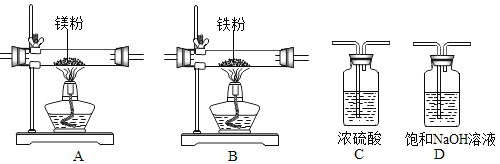
(2)通气后,应先点燃_____(填“A”或“B”)装置的酒精灯,如果同时点燃A、B装置的酒精灯,对实验结果有何影响?_____。
(3)设计一个实验,验证产物是氮化镁:
实验操作和实验现象 | 实验结论 |
_____ | 产物是氮化镁 |
(4)思维拓展:空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO的质量却远大于Mg3N2的质量,请给出合理的解释_____。
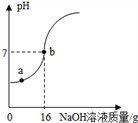
【题目】取一定量氯化镁溶液于烧杯中,将100g的氢氧化钠溶液平均分成五次加入烧杯中。在化学反应过程中对烧杯中的溶液和沉淀进行了多次过滤并称量。加入的氢氧化钠溶液和生成沉淀的质量关系记录如下表。
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
加入的氢氧化钠溶液质量/g | 20 | 20 | 20 | 20 | 20 |
沉淀总质量/g | 2.9 | 5.8 | 8.7 | 11.6 | 11.6 |
分析上表中的数据,完成下列问题:
(1)第_____次加完氢氧化钠溶液时,氯化镁和氢氧化钠恰好完全反应,此时生成沉淀质量为_____g。
(2)恰好完全反应时,称量所得氯化钠溶液质量为168.4g,则原氯化镁溶液中溶质的质量分数是____(请写出计算过程)。