题目内容
【题目】下列说法错误的是
A.金刚石和石墨物理性质差异很大,是因为构成它们的碳原子的原子结构不同
B.二氧化碳能灭火,既利用了物理性质,又利用了化学性质
C.用墨写的字不易褪色,这是因为常温下碳的化学性质不活泼
D.用洗洁精清洗餐具上的油污,这是利用洗洁精具有乳化功能
【答案】A
【解析】A、金刚石和石墨物理性质有很大差异是因为它们的碳原子排列不同,错误;
B、二氧化碳一般情况下不能燃烧,也不支持燃烧且密度比空气密度大,二氧化碳用于灭火,既利用了它的物理性质、也利用了它的化学性质,正确;
C、用墨写的字不易褪色,这是因为常温下碳化学性质不活泼,正确;
D、用洗洁精清洗餐具上的油污,这是利用洗洁精具有乳化功能,正确.
故选A

 阅读快车系列答案
阅读快车系列答案【题目】(15分)某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究.
【查阅资料】
①生产原料粗盐中含有少量可溶性杂质(MgCl2和CaCl2)及不溶性杂质(不与酸反应).
②生产原理反应:NaCl+ NH3 + CO2 + H2O= NaHCO3↓+ NH4Cl,分离得晶体B,并使其充分受热,可分解制得纯碱,同时得到二氧化碳和水.
③氯化铵分解的化学方程式是NH4Cl △ NH3↑+HCl↑.
④部分生产流程如下图所示:
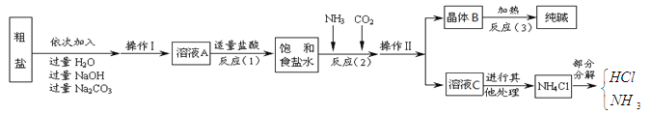
【问题讨论】
(1)①溶液A中的溶质有NaCl和 、 ,
②操作Ⅱ的名称为 .
③流程中Na2CO3溶液的作用是除去粗盐中的 .
④写出加入NaOH溶液与MgCl2反应的化学方程式 .
⑤晶体B受热分解的化学方程式为 .
(2)上述生产流程中可循环使用的是 (填序号).
A.NaOH B.NH3 C.HCl D.CO2
【组成探究一】
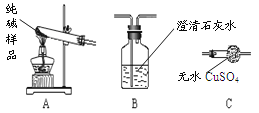
(3)设计实验检验纯碱样品中是否混有晶体B,请完成下表
选择的装置 | 实验现象 | 实验结论 |
选择的装置(填序号) | 实验现象 | 实验结论 |
样品不含晶体B |
【组成探究二】
(4)取纯碱样品加水溶解,向该溶液中加入过量稀HNO3,再滴加AgNO3溶液,有白色沉淀.产生沉淀的方程式为 ,由此确定纯碱样品含有杂质NaCl.
【组成探究三】
(5)同学们为了测定该纯碱样品的纯度,设计了如下实验:
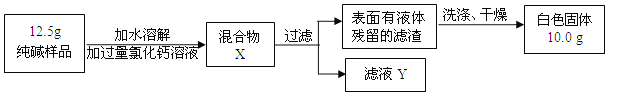
①判断加入氯化钙溶液是否过量的方法是 ,然后观察现象判断.
②判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,然后观察现象判断.
A.氯化钡溶液 B.硝酸银溶液 C.碳酸钠溶液 D.稀盐酸
③根据实验数据,计算样品中碳酸钠的质量分数是多少?(写出计算过程.3分)