题目内容
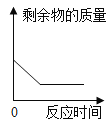
【题目】溶室喷头长时间使用会有白色固体附着,俗称水垢,这是因为硬水中含有较多的可溶性的碳酸氢钙[Ca(HCO3)2],还含有可溶性的碳酸氢镁[Mg(HCO3)2]。査阅资料,加热时会产生难溶性的固体。其中碳酸氢钙[Ca(HCO3)2]受热易分解生成难溶性的化合物、气体等物质。某小组想探究碳酸氢钙受热分解后产物的成分.
(提出猜想)猜想1.难溶性化合物可能是CaCO3;猜想2.气体可能是H2、CO、CO2。
(方案设计)请你设计实验,帮助该组同字确定难溶物的成分。
实验步骤 | 实验现象 | 结论 |
________________ | ________________ | 难溶物是CaCO3 |
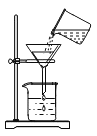
(实验探究)该组同学设计如图1实验,继续探究气体的成分。
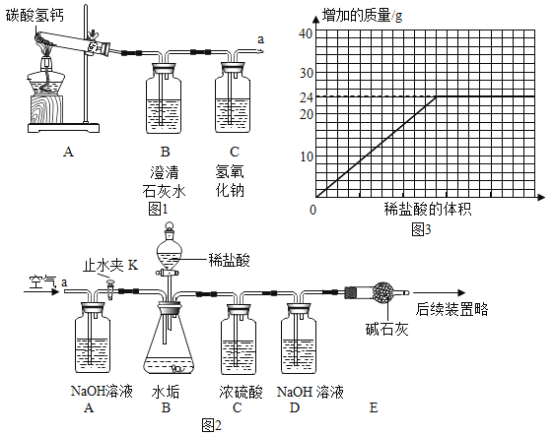
操作1.加热A装置,一段时间后,B装置中的澄清石灰水变浑浊。
操作2.在a处用燃着的木条检验,无明显现象
(实验结论)结论1.碳酸氢钙分解产生的气体是________结论2.碳酸氢钙受热分解的化学方程式为________________。
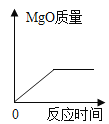
(反思评价)有同学提出:硬水中可溶性的碳酸氢镁[Mg(HCO3)2]受热也会产生不溶性的固体,那水垢的成分中还有什么物质?根据上述探究,该组同学设计如图2装置进一步实验。(已知碱石灰主要成分为CaO)和NaOH)。
(实验测定)步骤如下:
①按图组装仪器,先_______再将50g水垢样品放入锥形瓶中;
②打开止水夹K,从导管a处缓缓鼓入一定量的空气;
③逐滴加入足量稀盐酸,待锥形瓶中出现______________现象时,停止滴加稀盐酸;
④打开止水夹K,从导管a处缓缓鼓入一定量的空气;
⑤称量D瓶内物质增加的质量,直至D瓶内物质质量不变;
⑥测量滴加稀盐酸体积与D瓶内物质增加质量的关系如图3曲线所示。
(讨论交流)
①A装置中的NaOH溶液的作用是______________若没有A装置,D装置中的质量将______________(填“偏大”“不変”或“偏小”)。
②C装置中浓硫酸的作用是______________E装置的作用是______________。
③分析曲线图,通过计算可知:水垢中一定含有______________(填化学式),理由是____________________。
【答案】取少量难溶物于试管中,加入盐酸后,将产生的气体通入澄清石灰水 有气泡生成且石灰水变浑浊 二氧化碳 ![]() 检查装置气密性 不再产生气泡 吸收空气中的二氧化碳,以除去空气二氧化碳防止对后面测定的影响 偏大 吸收混在二氧化碳气体中的水的作用 避免空气中的二氧化碳进入E装置
检查装置气密性 不再产生气泡 吸收空气中的二氧化碳,以除去空气二氧化碳防止对后面测定的影响 偏大 吸收混在二氧化碳气体中的水的作用 避免空气中的二氧化碳进入E装置 ![]() 如果50g水垢全部为CaCO3,产生CO2的质量应为22g,而实验测得生成的CO2质量为24g,大于了22g
如果50g水垢全部为CaCO3,产生CO2的质量应为22g,而实验测得生成的CO2质量为24g,大于了22g
【解析】
稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊,碳酸氢钙加热生成碳酸钙、水和二氧化碳。
[方案设计]稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,二氧化碳能使澄清石灰水变浑浊。
实验步骤 | 实验现象 | 结论 |
取少量难溶物于试管中,加入盐酸后,将产生的气体通入澄清石灰水 | 有气泡生成且石灰水变浑浊 | 难溶物是CaCO3 |
[实验结论]结论1. 碳酸氢钙加热生成碳酸钙、水和二氧化碳,故碳酸氢钙分解产生的气体是二氧化碳。
结论2.碳酸氢钙受热分解的化学方程式为![]() 。
。
[实验测定]步骤如下:
①实验前,先要检查装置是否漏气,再按图组装仪器,先检查装置气密性再将50g水垢样品放入锥形瓶中;
③稀盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,逐滴加入足量稀盐酸,待锥形瓶中出现不再产生气泡现象时,停止滴加稀盐酸。
[讨论交流]
①二氧化碳和氢氧化钠反应生成碳酸钠和水,故A装置中的NaOH溶液的作用是吸收空气中的二氧化碳,以除去空气二氧化碳防止对后面测定的影响,若没有A装置,D装置中的质量将偏大。
②浓硫酸具有吸水性,故C装置中浓硫酸的作用是吸收混在二氧化碳气体中的水的作用,E装置的作用是以免空气中的二氧化碳被E装置吸收。
③设50g碳酸钙完全反应生成二氧化碳气体质量为x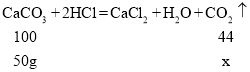
![]()
![]()
水垢完全反应放出二氧化碳的质量为24g>22g;碳酸钙、碳酸镁与盐酸反应放出二氧化碳的关系:等质量的碳酸镁与酸反应放出气体质量大于碳酸钙,水垢中应含有碳酸镁,化学式为![]() ,理由是如果50g水垢全部为CaCO3,产生CO2的质量应为22g,而实验测得生成的CO2质量为24g,大于了22g。
,理由是如果50g水垢全部为CaCO3,产生CO2的质量应为22g,而实验测得生成的CO2质量为24g,大于了22g。

 智慧小复习系列答案
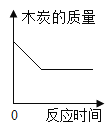
智慧小复习系列答案【题目】某化学兴趣小组探究浓硫酸与木炭反应后气体的成分。提出猜想:从物质组成元素角度分析,产生的气体可能是二氧化硫、二氧化碳和水。
查阅资料
(1)二氧化硫可使澄清石灰水变浑浊。
(2)二氧化硫可使品红溶液的红色褪去,而二氧化碳不能,以此检验二氧化硫。
(3)二氧化硫能被酸性高锰酸钾溶液吸收,而二氧化碳不能。
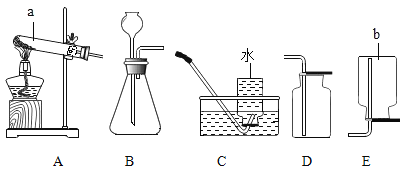
实验装置
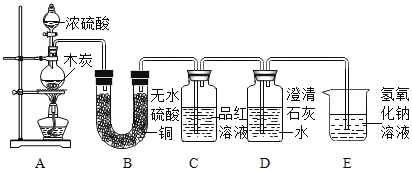
实验记录
序号 | 实验现象 | 实验结论 |
I | B中白色固体变成蓝色固体 | 产物中有水 |
II | C中品红溶液褪色 | 产物中有二氧化硫 |
III | D中澄清石灰水变浑浊 | 产物中有二氧化碳 |
交流与反思
(1)某同学认为结论 III不合理,原因是___________________。
(2)通过研究,小组对实验进行了改进:增加一个装有酸性高锰酸钾溶液的试剂瓶F.改进后实验装置的连接顺序为__________________________(填字母,实验装置可重复使用)。能确定产物中有二氧化碳的实验现象是________________________。
(3)经进一步确定,浓硫酸和木炭反应后的产物只有二氧化硫、二氧化碳和水,写出该反应的化学方程式______________________________。