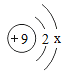题目内容
【题目】将等质量、颗粒大小相同的A、B两种金属分别同时投人到质量相等、溶质质量分数也相等的稀盐酸中,生成氢气的质量与时间的关系如图所示。已知两种金属在化合物中均显十2价,则下列说法不正确的是( )
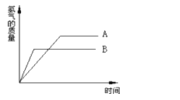
A.充分反应所需的时间:A>B
B.金属活动性:B>A
C.相对原子质量:A>B
D.A、B可能分别是常见金属中的Fe、Zn
【答案】C
【解析】
A、根据反应生成H2的质量与反应时间的关系图可知,等质量的金属B最先完全反应,A消耗的时间比B长,故A正确;
B、等质量的金属B最先完全反应,A消耗的时间比B长,两种金属中B的活动性较强,A较弱,故B正确;
C、一定质量的质量完全反应产生氢气的质量等于金属的化合价金属的相对原子质量乘以金属的质量,完全反应放出氢气的质量与金属的相对原子质量成反比,即产生氢气多的相对原子质量小,金属完全反应后,放出H2的质量是A>B,相对原子质量是B>A,故C不正确;
D、铁的相对原子质量小于锌,活泼性小于锌,A、B可能分别是常见金属中的Fe、Zn,故D正确。故选C。

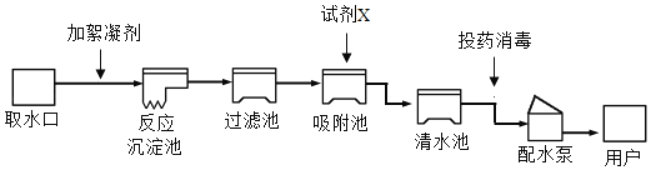
【题目】化学反应速率是衡量化学反应进行快慢的物理量。为了探究影响化学反应速率的因素,以过氧化氢分解为研究对象进行实验。其中一个小组采用如图装置进行实验,记录收集10mL氧气的时间。实验室可供选择的试剂有:10%浓度的![]() 溶液,
溶液,![]() 、
、![]() 、红砖粉末。
、红砖粉末。
探究:催化剂对化学反应速率的影响
取5mL10%![]() 溶液,三次实验分别加入0.5g
溶液,三次实验分别加入0.5g![]() 红砖粉末、
红砖粉末、![]() 进行实验,记录数据如下:
进行实验,记录数据如下:
试剂 |
| 红砖粉末 |
|
t/s | 10 | 60 | 20 |
由此得出结论;![]() 、
、![]() 对
对![]() 分解有催化作用,红砖粉末无催化作用。某同学对该结论提出疑问。补充对比实验,操作为___________________。结果:长时间(大于100s),收集到很少量气体。更正结论红砖粉末_______(选填“有”、“无”)催化作用,三者中_______催化效率高。
分解有催化作用,红砖粉末无催化作用。某同学对该结论提出疑问。补充对比实验,操作为___________________。结果:长时间(大于100s),收集到很少量气体。更正结论红砖粉末_______(选填“有”、“无”)催化作用,三者中_______催化效率高。
【题目】溶室喷头长时间使用会有白色固体附着,俗称水垢,这是因为硬水中含有较多的可溶性的碳酸氢钙[Ca(HCO3)2],还含有可溶性的碳酸氢镁[Mg(HCO3)2]。査阅资料,加热时会产生难溶性的固体。其中碳酸氢钙[Ca(HCO3)2]受热易分解生成难溶性的化合物、气体等物质。某小组想探究碳酸氢钙受热分解后产物的成分.
(提出猜想)猜想1.难溶性化合物可能是CaCO3;猜想2.气体可能是H2、CO、CO2。
(方案设计)请你设计实验,帮助该组同字确定难溶物的成分。
实验步骤 | 实验现象 | 结论 |
________________ | ________________ | 难溶物是CaCO3 |
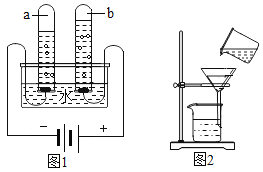
(实验探究)该组同学设计如图1实验,继续探究气体的成分。
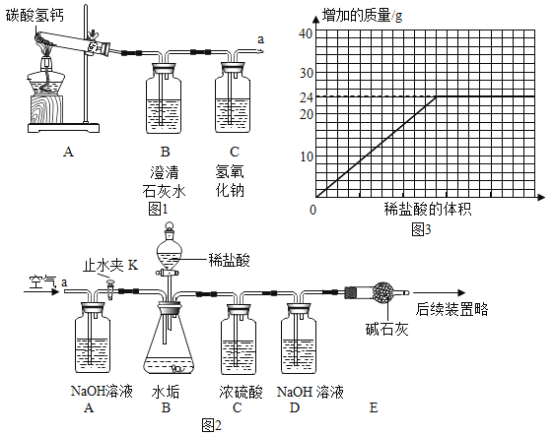
操作1.加热A装置,一段时间后,B装置中的澄清石灰水变浑浊。
操作2.在a处用燃着的木条检验,无明显现象
(实验结论)结论1.碳酸氢钙分解产生的气体是________结论2.碳酸氢钙受热分解的化学方程式为________________。
(反思评价)有同学提出:硬水中可溶性的碳酸氢镁[Mg(HCO3)2]受热也会产生不溶性的固体,那水垢的成分中还有什么物质?根据上述探究,该组同学设计如图2装置进一步实验。(已知碱石灰主要成分为CaO)和NaOH)。
(实验测定)步骤如下:
①按图组装仪器,先_______再将50g水垢样品放入锥形瓶中;
②打开止水夹K,从导管a处缓缓鼓入一定量的空气;
③逐滴加入足量稀盐酸,待锥形瓶中出现______________现象时,停止滴加稀盐酸;
④打开止水夹K,从导管a处缓缓鼓入一定量的空气;
⑤称量D瓶内物质增加的质量,直至D瓶内物质质量不变;
⑥测量滴加稀盐酸体积与D瓶内物质增加质量的关系如图3曲线所示。
(讨论交流)
①A装置中的NaOH溶液的作用是______________若没有A装置,D装置中的质量将______________(填“偏大”“不変”或“偏小”)。
②C装置中浓硫酸的作用是______________E装置的作用是______________。
③分析曲线图,通过计算可知:水垢中一定含有______________(填化学式),理由是____________________。
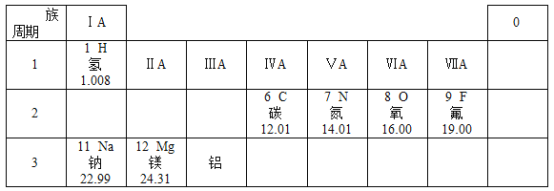
【题目】元素周期表是学习和研究化学的重要工具,它的内容十分丰富。如图是元素周期表的部分内容,请回答下列问题:
| I A | 0 | ||||||
1 | 1 H 1.008 | II A | III A | IV A | V A | VI A | VII A | 2 He 4.003 |
2 | 3 Li 6.941 | 4 Be 9.012 | 5 B 10.81 | 6 C 12.01 | 7 N 14.01 | 8 O 16.00 | 9 F 19.00 | 10 Ne 20.81 |
3 | 11 Na 22.99 | 12 Mg 24.31 | 13 Al 26.98 | 14 Si 28.09 | 15 P 30.97 | 16 S 32.06 | 17 Cl 35.45 | 18 Ar 39.95 |
(1)请从上表中查出地壳中含量最多的金属元素符号___________。
(2)8号元素和13号元素形成的化合物的化学式为________________。
(3)![]() 与Ar的核外电子排布相同,则
与Ar的核外电子排布相同,则![]() 的符号是___________。
的符号是___________。
(4)第3周期中属于金属元素的是___________(填一种),其阳离子符号是___________。
(5)不同元素的本质区别是___________。
(6)在元素周期表中,同一族的元素具有相似的化学性质,则下列各组元素具有相似化学性质的是__________(填序号)。
A C和Ne B Be和Mg C Al和Si D F和Cl
(7)具有相同原子数和电子数的分子或离子叫等电子体,下列各组粒子中属于等电子体的是__________(填序号)。
A NO和![]() B CO和
B CO和![]() C
C ![]() 和
和![]()