题目内容
【题目】下列有关化学反应与反应时间对应的图形不正确的是( )
A.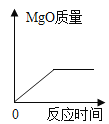 镁条点燃生成氧化镁的质量
镁条点燃生成氧化镁的质量
B.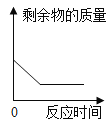 加热高锰酸钾制取氧气时剩余物的质量
加热高锰酸钾制取氧气时剩余物的质量
C.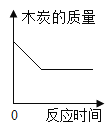 一定质量的木炭与过量氧气在密闭容器内加热使其充分反应
一定质量的木炭与过量氧气在密闭容器内加热使其充分反应
D. 过氧化氢分解制取氧气:(甲)加入二氧化锰(乙)稍微加热生成氧气质量
过氧化氢分解制取氧气:(甲)加入二氧化锰(乙)稍微加热生成氧气质量
【答案】C
【解析】
A、镁燃烧时,随着反应的进行,氧化镁的质量不断增加,当镁完全燃烧后,氧化镁的质量不再增加,化学反应与反应时间对应的图形正确;
B、加热高锰酸钾时,随着反应的进行,剩余物的质量不断减少,当反应完全后,质量不再减少,化学反应与反应时间对应的图形正确;
C、一定质量的木炭与过量氧气在密闭容器内加热使其充分反应,木炭的质量最终为0,化学反应与反应时间对应的图形不正确;
D、过氧化氢分解制取氧气时,催化剂能够加快反应速率,但是不影响生成氧气的质量,化学反应与反应时间对应的图形正确。
故选C。

【题目】实验室有一瓶黑色粉末和一瓶标签已被腐蚀的无色液体(如图)。将二者混合会产生无色气体。为了确定它们的成分,甲、乙两位同学进行了探究。
(查阅资料)
(1)铁粉末为黑色,化学性质与锌相似,与稀硫酸反应生成FeSO4和无色气体。
(2)碳与稀硫酸不发生化学反应。
(猜想1)甲同学认为无色气体是氧气,其理由是(用化学方程式表示):________。乙同学认为单从产生无色气体不能确定一定是氧气,需要进一步进行实验,请你设计实验进行验证无色气体是氧气。
实验步骤 | 实验现象 | 实验结论 |
__________ | __________ | 无色气体是氧气。 |
(猜想2)乙同学认为无色气体不一定是氧气,可能是其他气体,其理由是(用化学方程式表示)_________。
乙同学按自己的设想进行实验:取一定量的黑色粉末于试管中,加入过量的无色液体,当反应结束后,发现试管底部仍有黑色粉末。为确定此成分,请你设计实验进行验证:
实验步骤 | 实验现象 | 实验结论 |
1.将试管中的物质_______、洗涤、干燥。 2.点燃黑色粉末,在火焰上方罩一个涂有________的小烧杯。 | __________________ | 试管中剩余的黑色粉末可能是_______。 |
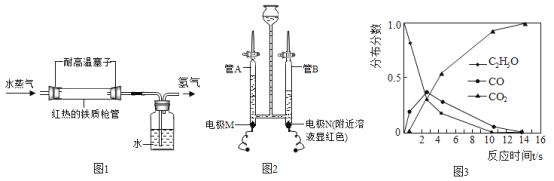
【题目】在老师的指导下,小华和小明利用如图1所示装置对氯酸钾制氧气进行了深入的探究学习。
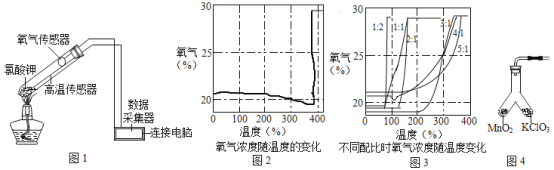
资料:①氯酸钾的熔点约为356℃,二氧化锰的分解温度约为535℃。用酒精灯给物质加热,受热物质的温度一般约为400℃左右;
②不同配比是指氯酸钾和二氧化锰混合物中,氯酸钾和二氧化锰的质量比;
③氯酸钾分解时,传感器得到氧气浓度随温度的变化示意图(图2)及不同配比时氧气浓度随温度的变化示意图(图3)如下:
请回答问题:
(1)分析图2,氯酸钾分解温度__________(填“高于”、“等于”或“低于”)其熔点。
(2)分析图2,在氯酸钾分解前,传感器得到氧气浓度降低的可能原因是_________________。
(3)分析图3,氯酸钾分解温度随物质配比变化的规律是_______________,当物质配比为1:2时,氯酸钾分解温度约为________℃。
(4)为证实二氧化锰的催化作用,小华利用如图4装置进行如表所示的实验:
步骤 | 实验操作 | 实验现象 |
Ⅰ | 检查气密性。 | |
Ⅱ | 分别在“Y”形管两侧支管中加入少量二氧化锰和氯酸钾,塞紧橡皮塞。 | |
Ⅲ | 分别用酒精灯先后加热二氧化锰和氯酸钾,用带火星木条放在导管口。 | 加热左侧支管,可观察到_____, 加热右侧支管,可观察到_____。 |
Ⅳ | 冷却后,将“Y”形管左侧支管中部分二氧化锰混入右侧支管中,振荡“Y”形管,加热,用带火星木条放在导管口。 | 加热时间短于步骤Ⅲ,木条很快复燃 |
请回答:
①完善步骤Ⅲ中的填空:加热左侧支管,可观察到______________,加热右侧支管,可观察到_________________。
②步骤Ⅳ中,将二氧化锰混入右侧支管有余热的氯酸钾中的操作方法是_______________。
③小华认为根据步骤Ⅳ的实验现象就能说明二氧化锰是氯酸钾分解的催化剂,但小明不同意她的观点,小明认为还需证明在此反应中二氧化锰的__________和__________不变。后来在老师的指导下,小华完善了实验方案,最终验证了自己的结论,则氯酸钾制取氧气的符号表达式__________________。