题目内容
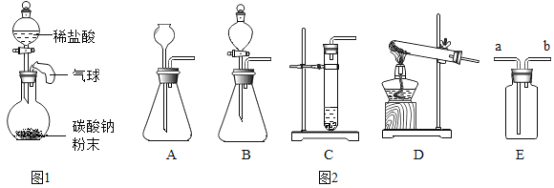
【题目】为探究酸的化学性质,某化学小组利用盐酸进行了如下实验操作,请回答
实验 |
A |
B |
C |
D |
E |
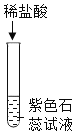
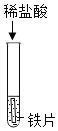
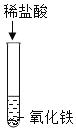
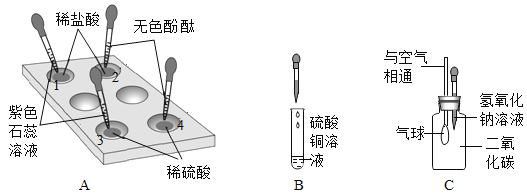
(1)A试管中的实验现象为___。写出图中C反应的化学方程式____。
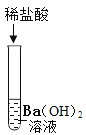
(2)将反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行如下探究:
(提出问题)滤液中溶质的成分是什么?
(作出猜想)
猜想一:NaCl
猜想二:NaCl和BaCl2
猜想三:NaCl、BaCl2和Na2CO3
猜想四:____。
(进行讨论)经过讨论,同学们一致认为猜想三是错误的.请用化学方程式解释其错误的原因_____________________。
(设计实验)请完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量的碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
取少量滤液于试管中,滴加稀硫酸 | ___ | 猜想四成立 |
(反思拓展)在分析反应后所得物质的成分时,除考虑生成物外还需考虑___。
【答案】溶液变红 Fe2O3+6HCl=2FeCl3+3H2O NaCl、Na2CO3 ![]() 有气泡产生 反应物是否过量(合理即可)
有气泡产生 反应物是否过量(合理即可)
【解析】
(1)A试管中是用稀盐酸滴加到紫色石蕊溶液,溶液变红色。图中C是稀盐酸与氧化铁反应生成氯化铁和水,反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O。
[作出猜想]
如果碳酸钠的量较多,氯化钡反应完,碳酸钠有剩余,则猜想四:NaCl、Na2CO3。
[进行讨论]
猜想三中既有氯化钡,又有碳酸钠,该猜想是错误的,因为氯化钡和碳酸钠会反应,不能共存于同一溶液中,反应方程式为![]() 。
。
[设计实验]
取少量滤液于试管中,滴加稀硫酸,可以验证猜想四成立,则滤液中含有氯化钠和碳酸钠,碳酸钠与稀硫酸反应生成硫酸钠、水和二氧化碳气体,故观察到有气泡产生。
[反思拓展]
通过以上实验分析,反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否过量。

 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
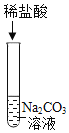
阳光考场单元测试卷系列答案【题目】实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是一种初中化学常用的试剂。小华等几位同学很感兴趣,决定对其成分进行探究。

(提出问题) 这瓶试剂含有的溶质是什么?
(交流研讨) 根据受损标签情况判断,这瓶试剂不可能是______(填序号)。
A. 酸 B.碱 C.盐
(查阅资料)①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
②Na2CO3、NaHCO3溶液都呈碱性。NaCl溶液呈中性。
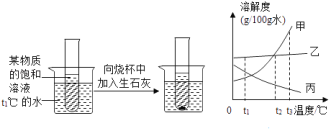
③室温下(20℃)时,4种物质的溶解度的数据如下。
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 36 | 109 | 215 | 9.6 |
(得出结论)小华根据试剂瓶标注和上表中的溶解度数据判断,这瓶试剂不可能是______。
(猜想与实验)①可能是______溶液; ②可能是Na2CO3溶液;③可能是NaCl溶液。
(1)小亮用洁净的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=11,他判断该溶液不可能是氯化钠。对他的操作方法、测量结果及结论的评价,正确的是______;
A.方法正确,结果正确,且结论正确 B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确 D.方法正确,结果正确,但结论不正确
(2)小强为了确定该溶液的成分,进行了如下实验。
操作步骤 | 实验现象 | 结论及化学方程式 |
步骤一: 取样品于试管中, 滴加足量__________ | 产生大量的气泡 | 猜想②正确。 步骤一发生反应的化学方程式是__________________ |
步骤二:把产生的气体,通入______ | ______________ |
(质 疑)小华则不同意小强的观点,认为溶液中Na2CO3是变质而来的,溶液中还可能有NaOH。请你帮助他完成以下探究方案
探究步骤 | 预计现象 | 结论 |
步骤一:取样品于试管中,向其中滴加足量的______溶液并过滤 | 产生白色沉淀 | 溶液中: 既含有Na2CO3, 又含有NaOH |
步骤二:向上述滤液中滴加酚酞试液 | 酚酞试液变______色 |
(反 思)NaOH溶液因接触空气而发生变质,写出该反应的化学方程式___________;配制10%的NaOH溶液时,应将氢氧化钠固体盛放于天平左盘的________中称量。