题目内容
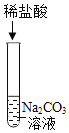
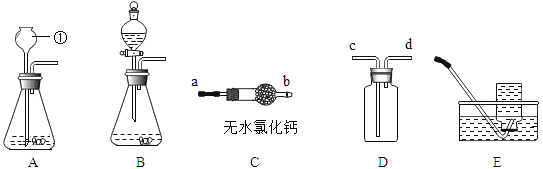
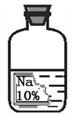
【题目】实验室有一瓶保存不当的试剂(如图所示),其残缺的标签中只剩下“Na”和“10%”字样。已知它是无色液体,是一种初中化学常用的试剂。小华等几位同学很感兴趣,决定对其成分进行探究。
(提出问题) 这瓶试剂含有的溶质是什么?
(交流研讨) 根据受损标签情况判断,这瓶试剂不可能是______(填序号)。
A. 酸 B.碱 C.盐
(查阅资料)①初中化学常见的含钠化合物有NaCl、NaOH、Na2CO3、NaHCO3。
②Na2CO3、NaHCO3溶液都呈碱性。NaCl溶液呈中性。
③室温下(20℃)时,4种物质的溶解度的数据如下。
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 36 | 109 | 215 | 9.6 |
(得出结论)小华根据试剂瓶标注和上表中的溶解度数据判断,这瓶试剂不可能是______。
(猜想与实验)①可能是______溶液; ②可能是Na2CO3溶液;③可能是NaCl溶液。
(1)小亮用洁净的玻璃棒蘸取该溶液滴到湿润的pH试纸上,测得pH=11,他判断该溶液不可能是氯化钠。对他的操作方法、测量结果及结论的评价,正确的是______;
A.方法正确,结果正确,且结论正确 B.方法不正确,结果偏小,但结论正确
C.方法不正确,结果偏大,结论不正确 D.方法正确,结果正确,但结论不正确
(2)小强为了确定该溶液的成分,进行了如下实验。
操作步骤 | 实验现象 | 结论及化学方程式 |
步骤一: 取样品于试管中, 滴加足量__________ | 产生大量的气泡 | 猜想②正确。 步骤一发生反应的化学方程式是__________________ |
步骤二:把产生的气体,通入______ | ______________ |
(质 疑)小华则不同意小强的观点,认为溶液中Na2CO3是变质而来的,溶液中还可能有NaOH。请你帮助他完成以下探究方案
探究步骤 | 预计现象 | 结论 |
步骤一:取样品于试管中,向其中滴加足量的______溶液并过滤 | 产生白色沉淀 | 溶液中: 既含有Na2CO3, 又含有NaOH |
步骤二:向上述滤液中滴加酚酞试液 | 酚酞试液变______色 |
(反 思)NaOH溶液因接触空气而发生变质,写出该反应的化学方程式___________;配制10%的NaOH溶液时,应将氢氧化钠固体盛放于天平左盘的________中称量。
【答案】A NaHCO3 NaOH B 稀盐酸 Na2CO3+2HCl===2NaCl+CO2↑+H2O 澄清石灰水 变浑浊 CaCl2(或BaCl2等) 红 CO2+ 2NaOH====Na2CO3+H2O 小烧杯(或表面皿或玻璃器皿)
【解析】
(1)酸的化学式开头都是氢元素,所以根据受损标签情况判断,这瓶试剂不可能是酸;(2)由题中信息可知NaHCO3的溶解度为9.6g,溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量。饱和溶液溶质的质量分数=溶解度÷(溶解度+100g)×100% ,所以 NaHCO3的溶液的溶质质量分数不可能达到10%;(3)由化学式可知可能是氢氧化钠溶液;(4)测溶液的pH,不能用湿润的pH试纸上,否则会因被稀释使碱性变弱,测定结果偏小;测得pH=11,数值合理,所以该溶液不可能是氯化钠。(5)碳酸钠能与酸反应生成二氧化气体,而冒气泡,反应的方程式为Na2CO3+2HCl===2NaCl+CO2↑+H2O;(7)验证二氧化碳的方法:将气体通入澄清石灰水中,澄清的石灰水变浑浊,证明气体是二氧化碳;(9)取样品于试管中,向其中滴加足量的氯化钙溶液(或BaCl2等其它合理试剂)并过滤,通过生成沉淀达到验证并除尽碳酸钠的目的;如果有氢氧化钠,则上述反应后的溶液呈碱性,加酚酞试液,溶液会变成红色;NaOH溶液因接触空气中二氧化碳发生反应生成碳酸钠而变质;(12)氢氧化钠固体易潮解,且腐蚀性非常强,常放在玻璃容器(烧杯)中称量。

 期末集结号系列答案
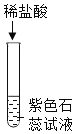
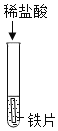
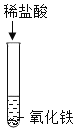
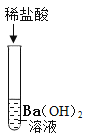
期末集结号系列答案【题目】为探究酸的化学性质,某化学小组利用盐酸进行了如下实验操作,请回答
实验 |
A |
B |
C |
D |
E |
(1)A试管中的实验现象为___。写出图中C反应的化学方程式____。
(2)将反应后D、E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行如下探究:
(提出问题)滤液中溶质的成分是什么?
(作出猜想)
猜想一:NaCl
猜想二:NaCl和BaCl2
猜想三:NaCl、BaCl2和Na2CO3
猜想四:____。
(进行讨论)经过讨论,同学们一致认为猜想三是错误的.请用化学方程式解释其错误的原因_____________________。
(设计实验)请完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量的碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
取少量滤液于试管中,滴加稀硫酸 | ___ | 猜想四成立 |
(反思拓展)在分析反应后所得物质的成分时,除考虑生成物外还需考虑___。
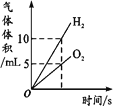
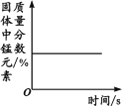
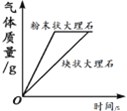
【题目】下列图像不能正确反映对应变化关系的是
|
|
|
|
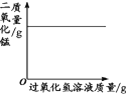
A.将水通电电解一 段时间 | B.加热一定量的高 锰酸钾固体 | C.向两份相等质量的块状大理石和粉末状大理石中分别加入过量的等浓度的稀盐酸 | D.向一定量的二氧化锰中加入过氧化氢溶液 |
A. A B. B C. C D. D