题目内容
【题目】金属材料包括纯金属以及它们的合金。
(1)在金属中加热熔合某些___,就可以制得具有金属特征的合金。
(2)铁制品锈蚀的过程,实际上是铁与空气中的___发生化学反应的过程。
(3)焊锡(锡铅合金)主要用于焊接金属,武德合金(铅、铋、锡和镉组成的合金)可用于制电路保险丝。根据下表提供的数据,可知合金的熔点一般___。
金属材料 | 纯金属 | 合金 | ||||
铅 | 镉 | 铋 | 锡 | 焊锡 | 武德合金 | |
熔点/℃ | 327 | 321 | 271 | 232 | 183 | 70 |
(4)1756年,俄国化学家罗蒙诺索夫把锡(Sn)放在密闭容器里煅烧,发现容器和容器里的物质的总质量在煅烧前后并没有发生变化。
①锡煅烧生成一种氧化物,其中锡元素的化合价为+4,该氧化物的化学式为___。
②罗蒙诺索夫认为在化学变化中物质的质量是守恒的。除了物质的质量以外,化学反应前后肯定没有变化的是___(填字母)。
A 原子数目 B 分子数目 C 原子种类 D 元素种类
(5)铁与硫酸铜溶液的反应在质量守恒定律的验证中起着重要的作用。若1.4g铁粉能与50g硫酸铜溶液恰好完全反应,则该硫酸铜溶液中溶质的质量分数是___?(写出计算过程)
【答案】金属或非金属 氧气、水蒸气等 低于组成它的纯金属 SnO2 ACD 8%
【解析】
(1) 由合金的定义可知,在金属中加热熔合某些金属或非金属,就可以制得具有金属特征的合金,故填写:金属或非金属;
(2) 铁制品锈蚀的过程,实际上是铁与空气中的氧气、水蒸气等发生化学反应的过程,故填写:氧气、水蒸气等;
(3)由表可知,合金的熔点一般低于组成它的纯金属,故填写:低于组成它的纯金属;
(4) 锡元素的化合价为+4,氧元素的化合价为-2,根据正负化合价为零的原则可得,该氧化物的化学式为SnO2,故填写:SnO2;
根据质量守恒定律的实质可得,化学反应前后肯定没有变化的是原子数目、原子种类和元素种类,故填写:ACD;
(5)解:设该硫酸铜溶液中溶质的质量为x
Fe+CuSO4=Cu+FeSO4
56 160
1.4g x
![]()
x=4g
硫酸铜溶液中溶质的质量分数是![]() ⅹ100%=8%
ⅹ100%=8%
答:该硫酸铜溶液中溶质的质量分数是8%

 小学课时特训系列答案
小学课时特训系列答案【题目】下列实验设计与结论对应关系正确的是( )
A | B | C | D | |
实 验 设 计 |
|
|
|
|
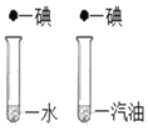
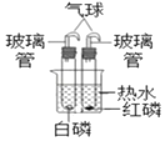
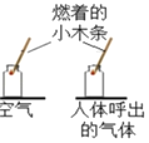
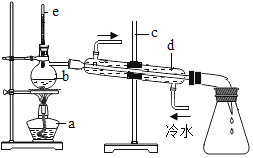
结 论 | 二氧化碳与水反应 | 不同的物质在同一溶剂中溶解性不同 | 燃烧的条件之一是温度达到可燃物的着火点 | 探究吸入气体和呼出气体中CO2的含量 |
A. AB. BC. CD. D