题目内容
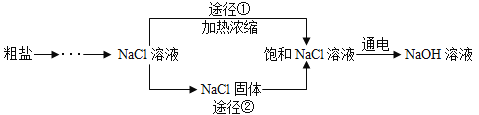
【题目】某同学设计的工业制备氢氧化钠的流程如图,下列说法正确的是( )
资料:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑,两电极一端得到NaOH和H2,另一端得到Cl2。
2NaOH+H2↑+Cl2↑,两电极一端得到NaOH和H2,另一端得到Cl2。
A. 晾晒海水得到粗盐的原理是降温结晶
B. 实验室测定水的组成时,为了增强水的导电性,可以在水中加入氯化钠
C. 工业生产应选择途径①进行生产,因为该途径步骤简单,节约能源
D. 生产过程中得到的Cl2可用于自来水的消毒杀菌
【答案】CD
【解析】
A、氯化钠的溶解度受温度变化影响较小,所以晾晒海水得到粗盐的原理是蒸发结晶,故A错误;
B、氯化钠和水在通电的条件下生成氢氧化钠、氢气和氯气,所以实验室测定水的组成时,为了增强水的导电性,可以在水中加入硫酸钠,故B错误;
C、工业生产应选择途径①进行生产氯化钠溶液的原理,因为该途径步骤简单,节约能源,故C正确;
D、氯气和水反应生成次氯酸和盐酸,次氯酸具有强氧化性,可以消毒,故D正确。
故选:CD。

【题目】金属材料包括纯金属以及它们的合金。
(1)在金属中加热熔合某些___,就可以制得具有金属特征的合金。
(2)铁制品锈蚀的过程,实际上是铁与空气中的___发生化学反应的过程。
(3)焊锡(锡铅合金)主要用于焊接金属,武德合金(铅、铋、锡和镉组成的合金)可用于制电路保险丝。根据下表提供的数据,可知合金的熔点一般___。
金属材料 | 纯金属 | 合金 | ||||
铅 | 镉 | 铋 | 锡 | 焊锡 | 武德合金 | |
熔点/℃ | 327 | 321 | 271 | 232 | 183 | 70 |
(4)1756年,俄国化学家罗蒙诺索夫把锡(Sn)放在密闭容器里煅烧,发现容器和容器里的物质的总质量在煅烧前后并没有发生变化。
①锡煅烧生成一种氧化物,其中锡元素的化合价为+4,该氧化物的化学式为___。
②罗蒙诺索夫认为在化学变化中物质的质量是守恒的。除了物质的质量以外,化学反应前后肯定没有变化的是___(填字母)。
A 原子数目 B 分子数目 C 原子种类 D 元素种类
(5)铁与硫酸铜溶液的反应在质量守恒定律的验证中起着重要的作用。若1.4g铁粉能与50g硫酸铜溶液恰好完全反应,则该硫酸铜溶液中溶质的质量分数是___?(写出计算过程)
【题目】某研究性学习小组以“酸与碱能否发生反应”为课题进行了实验探究。
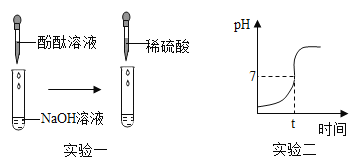
(实验一)
(1)向滴有酚酞试液的NaOH溶液中滴入稀硫酸,观察到溶液颜色由_____,证明硫酸和氢氧化钠发生了反应,该反应的化学方程式为_____。
(2)继续往上述反应后的溶液中逐滴滴入NaOH溶液,不断振荡,如果观察到_____现象,证明了滴加的稀硫酸过量。
(实验二)测量酸和碱反应过程的pH
(1)实验过程中用传感器实时获得溶液的pH,要得到如图所得变化曲线,所进行的操作是_____(填字母)。
A 将稀硫酸溶液逐滴滴加到氢氧化钠溶液中
B 将氢氧化钠溶液逐滴滴加到稀硫酸溶液中
(2)根据如图2溶液pH变化,判断酸和碱发生反应的依据是_____。
(实验三)小组同学经过讨论,一致认为除了上述方法外,还可以按照如表实验方法证明硫酸和氢氧化钠发生了反应。
实验步骤 | 实验现象 | 实验结论 |
取少量氢氧化钠溶液于试管中,加入过量的稀硫酸,再加入少量的氧化铜 | 得到蓝色溶液,无_____ | 氢氧化钠和硫酸发生了化 学反应 |
(拓展延伸)同学们对氢氧化钠溶液和稀硫酸反应后溶液中的溶质成分产生了浓厚的兴趣,于是进行了进一步的探究。
(提出问题)氢氧化钠溶液和稀硫酸反应后溶液中的溶质成分
(提出猜想)猜想一:Na2SO4猜想二:Na2SO4和H2SO4你的合理猜想是:_____。
(进行实验)
实验步骤 | 实验现象 | 实验结论 |
取少量反应后的溶液置于试管中_____ | _____ | 猜想二正确 |
(实验反思)在分析化学反应后所得物质成分时,除考虑生成物外还需要考虑反应物是否有剩余。
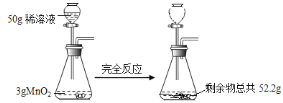
【题目】学习酸碱盐知识后,同学们知道碳酸钠溶液与氢氧化钙溶液能发生反应,可观察到溶液变浑浊。甲组同学进行如图所示的实验,却未观察到预期现象。
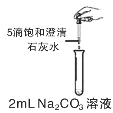
(提出问题)未观察到浑浊的原因是什么?
(猜想和假设)
①与氢氧化钙溶液的浓度有关。若使用更大浓度的氢氧化钙溶液,会迅速产生浑浊。
②与碳酸钠溶液的浓度有关。若使用更大浓度的碳酸钠溶液,会迅速产生浑浊。经讨论,同学们认为猜想①不合理,其理由是_______。
(进行实验)乙组同学针对猜想②进行实验。
实验目的 | 实验操作 | 实验现象 | |
探究猜想② | 取4支试管,向其中分别加入…… | 碳酸钠溶液浓度/% | 是否浑浊 |
10 | 不浑浊 | ||
5 | 不浑浊 | ||
1 | 浑浊 | ||
0.5 | 浑浊 | ||
(解释与结论)
(1)补全上述实验操作“……”部分:取4支试管,向其中分别加入2mL,浓度为10%,5%,1%,0.5%的碳酸钠溶液,再分别滴加_______。
(2)氢氧化钙溶液与碳酸钠溶液混合出现浑浊的化学方程式是_______。
(3)乙组实验证明:猜想②_____(填“成立”或“不成立”)。理由是_______。
(实验反思)
(4)丙组同学对乙组所做实验中未出现浑浊的原因进行探究。设计了多组实验,其中部分同学的实验过程及结果如下:
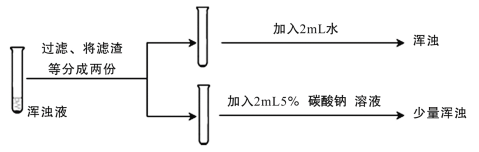
丙组同学的实验结论是_______。
(5)依据乙、丙两组的实验探究,丁组同学仍使用甲组的仪器和药品对甲组实验进行了改进,当滴入几滴某溶液后,溶液迅速变浑浊。其实验操作是_______