题目内容
【题目】实验室用石灰石和稀盐酸制取二氧化碳,并验证二氧化碳的性质。
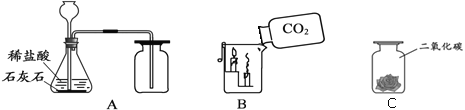
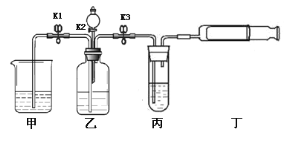
(1)A中制取气体的化学方程式为________;A装置还可用于实验室制取氧气,反应的化学方程式为______________。
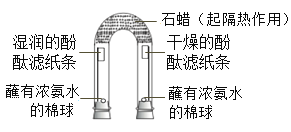
(2)实验B中,观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是____________。
(3)将紫色石蕊溶液浸泡并晾干的小花,一半喷水后放入集气瓶C中,该实验的目的是_____________________。
【答案】CaCO3+2HCl═CaCl2+H2O+CO2↑ 2H2O2![]() 2H2O+O2↑ 密度大于空气的密度,不能燃烧,不能支持燃烧 证明二氧化碳能与水反应
2H2O+O2↑ 密度大于空气的密度,不能燃烧,不能支持燃烧 证明二氧化碳能与水反应
【解析】
(1)A中制取气体为二氧化碳,反应原理是碳酸钙和盐酸反应生成二氧化碳、氯化钙、水,化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑;实验室中,过氧化氢法可用A装置制取氧气,反应原理是过氧化氢在二氧化锰的作用下分解生成水和氧气,化学方程式为2H2O2![]() 2H2O+O2↑;
2H2O+O2↑;
(2)实验B中,观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的性质是密度大于空气的密度,不能燃烧,不能支持燃烧;
(3)将紫色石蕊溶液浸泡并晾干的小花,一半喷水后放入集气瓶C中,该实验的目的是通过紫色石蕊试液变红,证明二氧化碳能与水反应。

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目