题目内容
【题目】砝码是化学实验室中的常用实验器材,如图所示是一盒砝码的实物图。请你回答下列问题:

(1)不锈钢属于________(填“单质”、“化合物”或“混合物”);图中属于合成材料的是________。
(2)砝码表面镀铬不仅美观,还可以防锈。铁锈主要成分的化学式是________,工业上常用________除去钢铁表面的铁锈。
(3)铬与浓硫酸发生反应的化学方程式为:![]() ,产生的
,产生的![]() 可用________性(填“酸”或“碱”)溶液来吸收,以减少对环境的污染。
可用________性(填“酸”或“碱”)溶液来吸收,以减少对环境的污染。
【答案】混合物 塑料(或海锦,写一种即可) ![]() 稀盐酸(或稀硫酸) 碱
稀盐酸(或稀硫酸) 碱
【解析】
(1)不锈钢是一种铁的合金,属于混合物;有机合成材料包括塑料、合成纤维和合成橡胶,故填:混合物;海绵(或塑料);
(2)铁锈的主要成分是氧化铁,氧化铁能与稀盐酸或稀硫酸反应,因此可用稀盐酸或稀硫酸来除铁锈;故填:Fe2O3;稀盐酸;
(3)产生的SO2可用碱溶液,如氢氧化钠溶液来吸收,以减少对环境的污染。故填:碱。

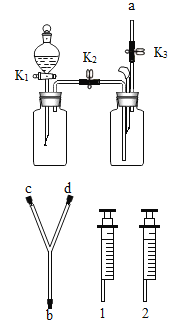
【题目】利用如图装置进行实验。实验前K1、K2、K3均已关闭。
内容 装置 | (实验1)探究燃烧条件 | (实验2)探究CO2与NaOH反应 |
| Ⅰ. A中加入少量的MnO2固体,分液漏斗中盛有H2O2溶液。 Ⅱ. B中长导管口处放置盛有白磷的容器,注入80℃的热水,至液面浸没下端导管口。 | Ⅰ. A中加入适量的Na2CO3固体,分液漏斗中盛放稀H2SO4溶液。 Ⅱ. 注射器1和2中分别是NaOH溶液和稀盐酸 |
(1)检查装置气密性:保持K1关闭,打开K2、K3,向B中加水至液面浸没下端导管口,用手捂住A瓶外壁,说明装置的左侧气密性良好的现象是________;用其他方法检验右侧气密性良好。
(2)实验1中,加入H2O2溶液前,水中的白磷不燃烧;打开K1、K2和K3,将H2O2溶液加入A中,关闭K1,观察到________,证明燃烧的条件之一是可燃物与氧气接触,B中发生反应的化学方程式为________________。
(3)实验2中,打开K1、K2、K3,向A中注入适量的稀H2SO4,关闭K1,一段时间之后,用燃着的木条放在a口处,木条熄灭,关闭K2, 上述实验操作的目的是______。此时,将装置B的a接口和Y型管的b接口连接,将注射器1中的溶液推入到B中,观察到气球明显变瘪;为进一步证明二氧化碳和氢氧化钠确实发生了反应,后续实验的操作及现象是_________________。
【题目】下表是NaC1、NH4Cl在不同温度时的溶解度,请回答问题
温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | |
溶解度(g) | NaC1 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 |
NH4C1 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | |
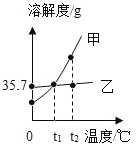
(1)30℃时,NaC1溶质质量分数的最大值是_____。
(2)NaC1和NH4C1溶解度相等时,对应温度的最小范围为_____。
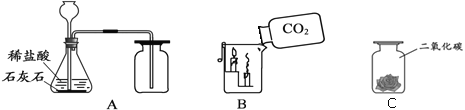
(3)如图所示,A是60℃时含有120g水的NH4C1溶液,经过如图操作后,得到固体。
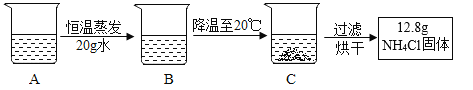
C中溶液质量是_____g,A溶液为NH4C1的_____(选填“饱和”或“不饱和”)溶液。
【题目】科学实践活动为同学们创设了独立思考和实践的机会。请完成下面小题。
【1】实践活动中,小亮自制了如图所示的净水器。
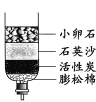
(1)此装置中活性炭的作用是____。
(2)使用此净水器净化的水属于_____。
A 纯净物 B 氧化物 C 化合物 D 混合物
【2】小明观察到了下列奇特的燃烧现象
|
|
图1:烧不坏的手帕 | 图2:“火龙生字”的纸 |
(1)点燃用白酒(含酒精56%)浸透过的手帕,“手帕”迅速燃烧起来,过一会儿,火熄灭了,但手帕却安然无恙,“烧不坏的手帕”的原因是_____。
(2)用带火星的木条轻轻地接触纸上用毛笔蘸饱和硝酸钾溶液写下的“火”字(已晾干),立即有火花出现,并缓慢地沿着字的笔迹蔓延,最后,在纸上呈现出用毛笔所写的“火”字,“火龙生字”的原因是_____。(提示:硝酸钾在受热条件下不稳定)