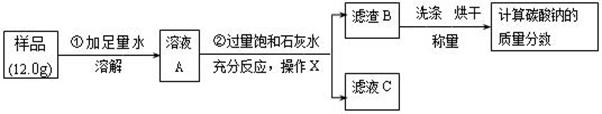
题目内容
将117.0g氯化钠溶液与140.0g的硝酸银溶液混合,恰好完全反应,过滤后所得溶液的质量为228.3g。计算该氯化钠溶液的溶质质量分数?
(反应的化学方程式为NaCl+AgNO3=AgCl↓+NaNO3)
解:根据质量守恒定律,生成AgCl的质量为117.0g+140.0g-228.3g=28.7g……(1分)
设原溶液中氯化钠的质量为x
NaCl+AgNO3=AgCl↓+NaNO3
58.5 143.5
X 28.7 g ……(1分)
……(1分)
x="11.7g" …………(1分)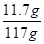 ×100%=10.0%…………(1分)
×100%=10.0%…………(1分)
答:氯化钠溶液的溶质质量分数是10.0% .
解析试题分析:根据过滤后所得溶液的质量可以计算氯化银沉淀的质量,根据氯化银的质量利用化学方程式可以计算氯化钠的质量,进一步可以计算该氯化钠溶液的溶质质量分数.
考点:根据化学反应方程式的计算;有关溶质质量分数的简单计算

练习册系列答案
 高中必刷题系列答案
高中必刷题系列答案
相关题目
同学们从山上采集到一种石灰石,他们取80克该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),测得反应后固体的质量(m)与反应时间(t)的关系如下表:
| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 80 | 75 | 70 | 66 | 62 | 58 | 58 |
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为 g。
(2)求该石灰石中CaCO3的质量分数,写出计算过程。
有一种石灰石样品的成分是CaCO3和SiO2。课外小组同学将100g盐酸分5次加入到35g该石灰石样品中(已知SiO2不与盐酸反应),得到如下部分数据和图像:
| 次数 | 第1次 | 第2次 | 第3次 |
| 加入盐酸的质量/g | 20 | 20 | 20 |
| 剩余固体的质量/g | 30 | a | 20 |
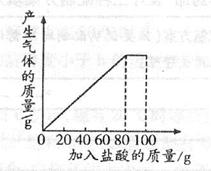
请计算:
(1)第2次加入盐酸后,a为 g;
(2)石灰石样品中碳酸钙的质量分数;(计算结果精确至0.1%)
(3)10%的CaCl2溶液可做路面保湿剂。欲将第5次实验后的溶液配成10%的CaCl2溶液,可先向此溶液中加入足量的石灰石粉末,完全反应后过滤,这时还需要向滤液中加入水多少克?(假设实验过程中溶液损失忽略不计)(计算结果精确至0.1g)