题目内容
((7分)某纯碱样品中混有少量的氯化钠,为了测定该样品中碳酸钠的质量分数,小明同学准确称取 12.0g样品,做了如下实验: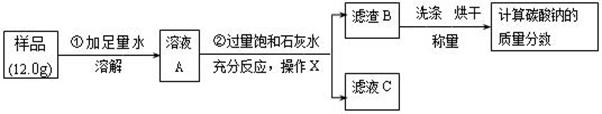
请回答下列问题:
(1)操作X用到的玻璃仪器除烧杯、玻璃棒外,还必需有 。
(2)滤液 C中的溶质是 ,若向滤液 C中滴加稀盐酸,写出过程中发生的一个中和反应的化学方程式 。
(3)若将滤渣B洗涤烘干后,称量其质量为 10.0g , 计算纯碱样品中的 Na2CO3的质量分数是多少?(结果保留一位小数,要求写出计算过程)
(1)漏斗(或普通漏斗)(2)氯化钠、氢氧化钠、氢氧化钙(写化学式也可,少答得1分、错答不给分);NaOH + HCl ="=" NaCl + H2O【或Ca(OH)2 + 2HCl ="=" CaCl2 +2H2O】
(3)88.3%
解析试题分析:(1)操作X是物质分为滤渣B和滤液C,所以操作应为过滤;用到的玻璃仪器除烧杯、玻璃棒外,还必需有漏斗。
(2)碳酸钠和氢氧化钙(石灰水的溶质)反应生成碳酸钙沉淀和氢氧化钠;所以滤液 C中的溶质有氢氧化钠;石灰水过量,则滤液C中还含有未反应的氢氧化钙;原样品中的氯化钠未发生反应,可进入滤液C中。所以滤液C中的成分为氢氧化钠、氢氧化钙和氯化钠。
若向滤液 C中滴加稀盐酸,则反应有:NaOH + HCl ="=" NaCl + H2O和Ca(OH)2 + 2HCl ="=" CaCl2 +2H2O。
(3)根据题意可知,已知量为滤渣B(碳酸钙)质量为 10.0g;未知量为样品中的 Na2CO3的质量分数。
解题思路:可根据碳酸钙和碳酸钠在反应中的质量关系,求出碳酸钠的质量,再进一步求出其质量分数。具体过程如下:
解:设要生成10.0g碳酸钙需要碳酸钠的质量为x
Na2CO3 + Ca(OH)2 = CaCO3↓+ 2NaOH
106 100
x 10.0g
106 : 100 =" x" :10.0g
X=10.6g
样品中碳酸钠的质量分数为: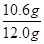 ×100% =" 88.3%"
×100% =" 88.3%"
答:样品中碳酸钠的质量分数为88.3%
考点:除杂、综合计算

 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案(7分)为测定某纯碱样品(含氢氧化钠杂质)中碳酸钠的含量,进行如下实验:取65g纯碱样品平均分为5份,分别加入相同质量分数的稀盐酸溶液,获得如下实验数据:
| 实验 | 1 | 2 | 3 | 4 | 5 |
| 样品质量/g | 13 | 13 | 13 | 13 | 13 |
| 加入盐酸质量/g | 15 | 30 | 80 | 130 | 150 |
| 反应后物质质量/g | 28 | 43 | 90.8 | 138.6 | 158.6 |
(2)纯碱样品中Na2CO3的质量分数是多少?(写出计算过程,结果保留小数点后一位)
(3)13g样品与盐酸恰好完全反应后生成物溶液中溶质的质量分数是 。(只写结果,保留小数点后一位)
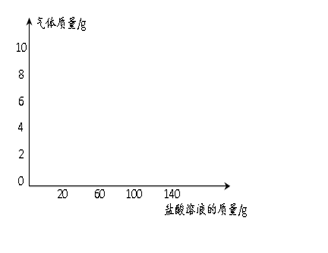
(4)若向13g样品中持续不断的加入稀盐酸,请你画出加入稀盐酸与生成气体的质量关系图。(在答题卡的坐标中作图)