题目内容
【题目】向盛有60g 15%的氢氧化钡溶液的烧杯中,缓慢滴加稀硫酸至过量。烧杯中的某些量随着稀硫酸的滴加,其变化趋势肯定错误的是( )
A. 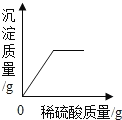 B.
B. 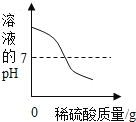
C. 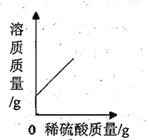 D.
D. 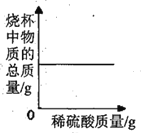
【答案】C
【解析】
A、向盛有60g 15%的氢氧化钡溶液的烧杯中,缓慢滴加稀硫酸至过量,氢氧化钡溶液与稀硫酸反应生成硫酸钡沉淀和水,沉淀的质量逐渐增加,至完全反应不再发生改变,故选项图象变化趋势正确;
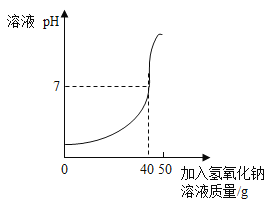
B、向盛有60g 15%的氢氧化钡溶液的烧杯中,缓慢滴加稀硫酸至过量,碱性逐渐变弱,酸性逐渐增强,pH值的变化是从大于7逐渐的减小到小于7,故选项图象变化趋势正确;
C、氢氧化钡溶液与稀硫酸反应生成硫酸钡沉淀和水,随着反应的进行,溶质质量逐渐减少,至完全反应减少至0,继续滴加稀硫酸,溶质质量又开始增加,故选项图象变化趋势错误;
D、该反应遵守质量守恒定律,反应前后烧杯中物质的总质量不变,故选项图象变化趋势正确。
故选C。

【题目】某化工厂用石灰石和废铜屑等设计生产石青、波尔多液的工艺流程如下:
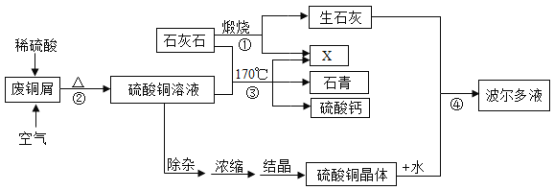
一、产品制备
(1)流程图中X的化学式为__________;
(2)反应②的总化学方程式为__________________________;
(3)硫酸铜晶体(CuSO45H2O)的溶解度如下表:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 80 | 100 |
溶解度/g | 14.3 | 17.4 | 20.7 | 25.0 | 28.5 | 33.3 | 40.0 | 55.0 | 75.4 |
蒸发浓缩后热溶液经处理大量析出晶体,温度到达30℃时,剩余硫酸铜溶液的溶质质量分数为_____;待结晶完毕后,滤出晶体,用少量冰水洗涤2﹣3次,用冰水洗涤的目的是:Ⅰ是除去晶体表面的杂质;Ⅱ是___________________。
(4)反应④中硫酸铜、生石灰和水制备波尔多液,其化学方程式为:Ⅰ是_____________________;Ⅱ是___________________________。
二、组成测定
查阅资料:石青的化学式可表示为aCuCO3bCu(OH)2,Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃。为测定其组成,小组同学称取石青样品34.6g,用如图装置进行实验。
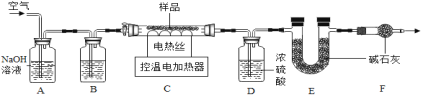
(5)洗气瓶A中氢氧化钠溶液的作用是_____;B中所装液体为_____。
(6)现控制C装置中的温度为250℃对石青进行热分解,直至C装置中剩余固体质量不再变化为止,再缓缓通入一段时间空气后,冷却后装置D增重1.8g,装置E增重8.8g.通过计算可得:a:b=_____。
(7)若缺少F装置,测得的a:b_____(选填“偏大”、“偏小”、“不变”)。
三、脱水探究
硫酸铜晶体受热会逐步失去结晶水.取纯净CuSO45H2O固体2.50g,放在如图实验装置C中进行加热,测定固体质量随温的变化情况如图所示。
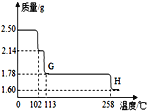
(8)G点固体的化学式是_____。
(9)G→H看到的现象是_____。
(10)将CuSO45H2O固体加热到570℃分解后,得到的主要产物是黑色粉末、硫的一种氧化物和水蒸气,该反应的化学方程式为:_____。