题目内容
【题目】请根据下列实验装置图,回答问题。
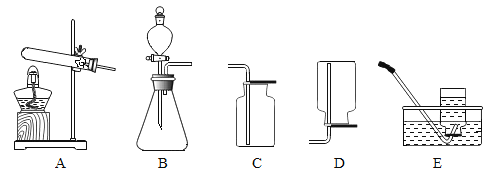
(1)实验室用双氧水和二氧化锰制取氧气的化学方程式为________________,发生装置为________(填字母序号)。若反应过于剧烈,从实验安全角度考虑,可以采取的措施有______________(写一种即可)。
(2)实验室用高锰酸钾制取氧气,为进一步研究高锰酸钾的分解产物,某兴趣小组查阅资料,并取一定质量的高锰酸钾加热使之完全分解,进行下表所示的实验。
(实验内容):
编号 | 实验内容 | 实验现象 | 实验结论 |
1 | 取反应后固体剩余物0.2g加入5mL%的H2O2溶液 | 剧烈反应,放热,产生大量气泡 | 生成物中的MnO2催化分解H2O2 |
2 | 取0. 2g MnO2加入5mL_____(填H2O2溶液的溶质质量分数)的H2O2溶液 | 平稳反应,放热,持续产生气泡 | MnO2催化分解H2O2 |
3 | 取反应后固体剩余物1. 0g,加入足量水,充分溶解,过滤 | 固体完全溶解,滤纸上无黑色固体残余物 | 固体剩余物中无_____ |
(实验分析):
①完善上表中的填空内容:实验2________,实验3________。
②实验2的目的是________。
③经讨论,实验1的结论不正确,理由是________。
(资料):在43.9℃~377.9℃范围中,KMnO4受热分解时,会发生以下两个反应:
a.![]()
b.![]()
④取8.0g KMnO4加热使之完全分解,生成O2的质量可能为________(填字母序号);
A0.81 g B1.08 g C1.42 g D1.62 g
⑤资料显示,KMnO4在43.9℃~377 .9℃范围中的失重率(O2与KMnO4的质量比)为18.0%。结合资料分析,在43.9℃~377.9℃范围中,KMnO4分解反应主要以____(填“a”或“b”)为主。
【答案】2H2O2![]() 2H2O+ O2↑ B 调节分液漏斗上的活塞,缓慢滴加过氧化氢溶液(合理即可) 6% 二氧化锰 和实验1进行对比,确定MnO2是否为起催化作用 可能是分解后产物中其他物质起催化作用 C b
2H2O+ O2↑ B 调节分液漏斗上的活塞,缓慢滴加过氧化氢溶液(合理即可) 6% 二氧化锰 和实验1进行对比,确定MnO2是否为起催化作用 可能是分解后产物中其他物质起催化作用 C b
【解析】
(1)过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,反应的化学方程式为:2H2O2![]() 2H2O+ O2↑;如果用双氧水和二氧化锰制氧气,反应物的状态是固体与液体,不需要加热,发生装置可选用B;若反应过于剧烈,从实验安全角度考虑,可以采取的措施有:调节分液漏斗上的活塞,缓慢滴加过氧化氢溶液或减小过氧化氢溶液的浓度等;
2H2O+ O2↑;如果用双氧水和二氧化锰制氧气,反应物的状态是固体与液体,不需要加热,发生装置可选用B;若反应过于剧烈,从实验安全角度考虑,可以采取的措施有:调节分液漏斗上的活塞,缓慢滴加过氧化氢溶液或减小过氧化氢溶液的浓度等;
(2)①实验2是与实验1对比,确定MnO2是否起催化作用,则所取H2O2溶液的溶质质量分数应相同。实验中应加入5mL6%的H2O2溶液,实验3取反应后固体剩余物1.0g加入足量水中,充分溶解,过滤后固体完全溶解,说明不含MnO2,因为MnO2不溶于水;
②实验2是与实验1作对比,确定MnO2是否起催化作用;
③由实验3可知反应产物中是否有MnO2,从而反映出实验1不严密,也可能是分解后的其他物质起催化作用;
④若发生的是a反应,设8.0gKMnO4,加热使之完全分解,生成O2的质量为x,则
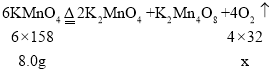
![]() x=1.08g,
x=1.08g,
若发生的是b反应,设8.0gKMnO4,加热使之完全分解,生成O2的质量为y,则
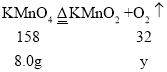
![]() ,y=1.62g,
,y=1.62g,
因为KMnO4受热分解,会发生以上两个反应,所以生成氧气的质量介于1.08g和1.62g之间,故C正确;
⑤由题意可知:KMnO4在43.9℃~377.9℃范围中的失重率(O2与KMnO4质量比)为18.0%,据方程式可知:在a反应中失重率为:![]() ≈0.135,b反应中失重率为:
≈0.135,b反应中失重率为:![]() ≈0.201,可以发现,此时的失重率为18.0%,与b的失重率较为接近,故在43.9℃~377.9℃范围中,KMnO4分解反应主要以b为主。
≈0.201,可以发现,此时的失重率为18.0%,与b的失重率较为接近,故在43.9℃~377.9℃范围中,KMnO4分解反应主要以b为主。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】黄铜是铜和锌的合金。某化学兴趣小组的同学欲测定实验室中某黄铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程。称量10g粉末状黄铜样品放入烧杯中,量取45mL稀硫酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
第一次 | 第二次 | 第三次 | |
加入稀硫酸的体积(mL) | 15 | 15 | 15 |
生成氢气的质量(g) | m | 0.04 | 0.02 |
试求:
(1)m的数值_____。
(2)此黄铜样品中铜的质量分数是少?_____(写出计算过程)