题目内容
【题目】根据下列实验装置图,回答有关问题。

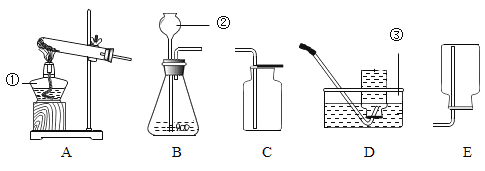
(1)装置图中仪器a的名称为___。
(2)用氯酸钾和二氧化锰混合制取氧气,可选用的发生装置是___(填字母),写出该反应的化学方程式___;若用D装置收集氧气,当导管口气泡___冒出时,再把导管口伸入盛满水的集气瓶。
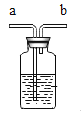
(3)实验室用B装置制取二氧化碳的化学方程式为___,如果用G装置收集气体,气体应从___(填“b”或“c”)端通入;用C装置代替B装置,收集所需的气体量后,对C装置进行的操作是___。
(4)水是生命之源,是“永远值得探究的物质”,人类从未停止过对水的研究。
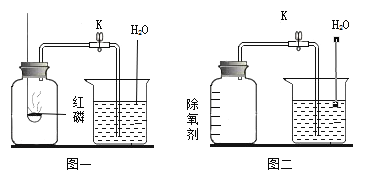
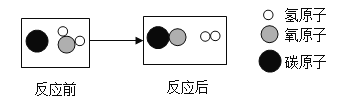
①1766年,英国化学家卡文迪许用锌和稀硫酸制得“可燃空气”,他所说的“可燃空气”成分是___(填化学式)。“可燃空气”在纯氧中燃烧生成水,可得出“水是一个结合物而不是简单元素”。
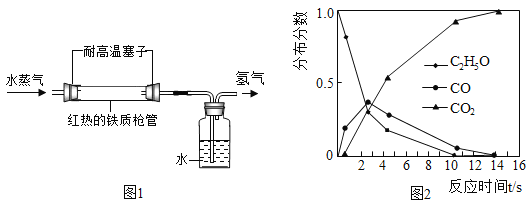
②1785年,拉瓦锡将水蒸气通过红热的铁制枪管将水转化为氢气,同时生成四氧化三铁,实验示意图如图1所示。上述反应的化学方程式为___。该反应若生成1g氢气,则理论上铁制枪管应增重___g。
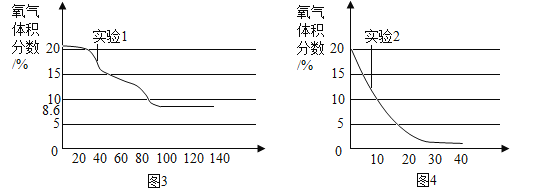
③当温度、压强分别超过临界温度(374.2℃)和临界压强(22.1MPa)时的水称为超临界水。现代研究表明:超临界水能够与氧气以任意比例互溶,由此发展了超临界水氧化技术。550℃时,测得乙醇(C2H6O)的超临界水氧化结果如图2所示。图中CO的分布分数先增后降的原因是___。
【答案】集气瓶 A ![]() 连续均匀
连续均匀 ![]() b 关闭止水夹 H2 3Fe+4H2O(g)
b 关闭止水夹 H2 3Fe+4H2O(g)![]() Fe3O4+4H2 8 C2H6O先被氧化成CO,后CO被氧化成CO2
Fe3O4+4H2 8 C2H6O先被氧化成CO,后CO被氧化成CO2
【解析】
(1)E为向上排空气法收集气体,a仪器的名称为集气瓶。
(2)氯酸钾在二氧化锰催化和加热的条件下产生氧气,发生装置为固固加热型,因此可选择A装置;产生的氧气可用排水法和向上排空气法收集,用D装置排水法收集,当导管口气泡连续均匀的冒出时,才能开始收集氧气,化学方程式为:![]() 。
。
(3)实验室用石灰石或大理石与稀盐酸反应制取二氧化碳,为固液不加热型反应;产生的二氧化碳密度比空气大,可溶于水,用G装置收集时,空气从上口排出,因此气体需要从b端通入;若用C装置代替,收集完后,将导管上的止水夹关闭即可停止收集。反应化学方程式为:![]() 。
。
(4)①锌和稀硫酸反应,产生氢气,可燃空气成分是氢气,化学式为:H2。
②将水蒸气通过红热的铁制枪管将水转化为氢气,同时生成四氧化三铁,化学方程式为:3Fe+4H2O(g)![]() Fe3O4+4H2。氢气的来源只有水,若该反应要生成1g氢气,设需要的水蒸气的质量为m:则有
Fe3O4+4H2。氢气的来源只有水,若该反应要生成1g氢气,设需要的水蒸气的质量为m:则有![]() ,因此增重的质量为9g-1g=8g。
,因此增重的质量为9g-1g=8g。
③550℃时,乙醇(C2H6O)的超临界水氧化结果如图2所示,图中CO的分布分数先增后降,可能原因是C2H6O先被氧化成CO,后CO与氧气反应,产生CO2,导致先增后降。

【题目】如图是取大小形状相同的Mg、Zn、Fe、Cu四种金属与相同浓度的稀盐酸反应状况的示意图.仔细观察并结合所学的知识回答下列问题:

(1)不能与稀盐酸反应的金属是__________.
(2)图中显示有三种金属能与稀盐酸反应,其共同的反应现象是___________,其中反应速率最快的是__________,请写出它与盐酸反应的化学方程式是_____________.
(3)通过以上实验(或图示)说明,Zn和Cu的金属活动性强弱是___________.
(4)某兴趣小组的同学为了探究哪些因素可以影响金属与酸溶液反应的速率设计并进行了如下实验:
序号 | 实验过程 | 实验现象 |
① | 锌粉和铁粉分别与10%______反应 | 锌粉产生气体的速率快 |
② | 铁粉和铁片分别与10%盐酸反应 | _____产生气体的速率快 |
③ | 铁片分别与5%和10%盐酸反应 | 10%盐酸产生气体的速率____ |
(5)通过上述实验,小组同学得出了影响金属与酸溶液反应的速率的因素有很多,请你写出其中的一种____________.此外同学们提出影响金属与酸溶液反应的速率的因素还可能有温度,温度越高,反应速率越_____________(填“快”或“慢”).
【题目】请根据下列实验装置图,回答问题。
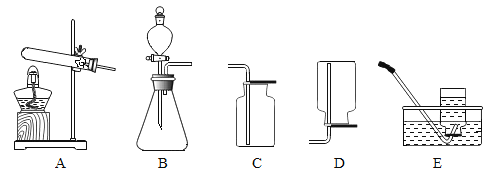
(1)实验室用双氧水和二氧化锰制取氧气的化学方程式为________________,发生装置为________(填字母序号)。若反应过于剧烈,从实验安全角度考虑,可以采取的措施有______________(写一种即可)。
(2)实验室用高锰酸钾制取氧气,为进一步研究高锰酸钾的分解产物,某兴趣小组查阅资料,并取一定质量的高锰酸钾加热使之完全分解,进行下表所示的实验。
(实验内容):
编号 | 实验内容 | 实验现象 | 实验结论 |
1 | 取反应后固体剩余物0.2g加入5mL%的H2O2溶液 | 剧烈反应,放热,产生大量气泡 | 生成物中的MnO2催化分解H2O2 |
2 | 取0. 2g MnO2加入5mL_____(填H2O2溶液的溶质质量分数)的H2O2溶液 | 平稳反应,放热,持续产生气泡 | MnO2催化分解H2O2 |
3 | 取反应后固体剩余物1. 0g,加入足量水,充分溶解,过滤 | 固体完全溶解,滤纸上无黑色固体残余物 | 固体剩余物中无_____ |
(实验分析):
①完善上表中的填空内容:实验2________,实验3________。
②实验2的目的是________。
③经讨论,实验1的结论不正确,理由是________。
(资料):在43.9℃~377.9℃范围中,KMnO4受热分解时,会发生以下两个反应:
a.![]()
b.![]()
④取8.0g KMnO4加热使之完全分解,生成O2的质量可能为________(填字母序号);
A0.81 g B1.08 g C1.42 g D1.62 g
⑤资料显示,KMnO4在43.9℃~377 .9℃范围中的失重率(O2与KMnO4的质量比)为18.0%。结合资料分析,在43.9℃~377.9℃范围中,KMnO4分解反应主要以____(填“a”或“b”)为主。