题目内容
【题目】联合国将2019年列为“国际化学元素周期表年”。锶、镁元素在元素周期表中的部分信息及原子结构示意图如下,请回答下列问题。

(1)镁元素的相对原子质量为______,属于______元素(填“金属”或“非金属”、“稀有气体”)。
(2)锶原子在化学反应中容易_____(填“得”或“失”)电子,锶的氧化物的化学式为_________。
(3)镁元素与锶元素的化学性质_________(填“相似”或“不相似”)。
【答案】24.31 金属 失 SrO 相似
【解析】
(1)除过金、汞以外,元素名称中含有“钅”字旁的元素属于金属元素;
(2)元素的化学性质与原子的最外层电子数有关,化合物中各组成元素的正负化合价代数和为0,据此分析。
(1)图A是元素周期表中关于元素镁的一格信息,汉字为元素名称,元素名称正下方的数字表示该元素的相对原子质量,则镁元素的相对原子质量为24.31;“镁”含有“钅”字旁,属于金属元素;
(2)由图D可知,锶原子的最外层电子数为2,小于4,因此锶原子在化学反应中容易失去2个电子,Sr在其氧化物中显+2价,则其氧化物的化学式为SrO;
(3)由图C、D可知,两种原子的最外层电子数均为2,则这两种元素的化学性质相似。

【题目】某密闭容器中有X、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表。根据表中信息,判断下列说法正确的是( )
物质 | X | O2 | CO2 | H2O |
反应前质量g | 16 | 70 | 1 | 0 |
反应后质量g | 0 | 待测 | 45 | 36 |
A.该反应为分解反应B.X中含有碳、氢、氧三种元素
C.生成的CO2和H2O的分子个数比为1:2D.生成的CO2和H2O的质量比为45:36
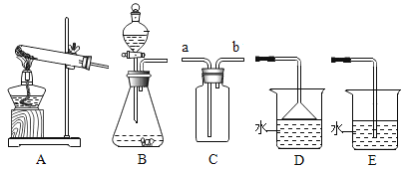
【题目】请根据下列实验装置图,回答问题。
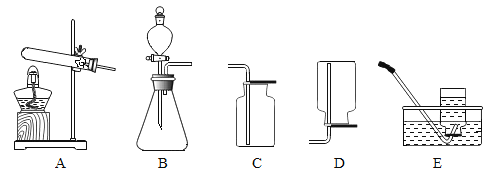
(1)实验室用双氧水和二氧化锰制取氧气的化学方程式为________________,发生装置为________(填字母序号)。若反应过于剧烈,从实验安全角度考虑,可以采取的措施有______________(写一种即可)。
(2)实验室用高锰酸钾制取氧气,为进一步研究高锰酸钾的分解产物,某兴趣小组查阅资料,并取一定质量的高锰酸钾加热使之完全分解,进行下表所示的实验。
(实验内容):
编号 | 实验内容 | 实验现象 | 实验结论 |
1 | 取反应后固体剩余物0.2g加入5mL%的H2O2溶液 | 剧烈反应,放热,产生大量气泡 | 生成物中的MnO2催化分解H2O2 |
2 | 取0. 2g MnO2加入5mL_____(填H2O2溶液的溶质质量分数)的H2O2溶液 | 平稳反应,放热,持续产生气泡 | MnO2催化分解H2O2 |
3 | 取反应后固体剩余物1. 0g,加入足量水,充分溶解,过滤 | 固体完全溶解,滤纸上无黑色固体残余物 | 固体剩余物中无_____ |
(实验分析):
①完善上表中的填空内容:实验2________,实验3________。
②实验2的目的是________。
③经讨论,实验1的结论不正确,理由是________。
(资料):在43.9℃~377.9℃范围中,KMnO4受热分解时,会发生以下两个反应:
a.![]()
b.![]()
④取8.0g KMnO4加热使之完全分解,生成O2的质量可能为________(填字母序号);
A0.81 g B1.08 g C1.42 g D1.62 g
⑤资料显示,KMnO4在43.9℃~377 .9℃范围中的失重率(O2与KMnO4的质量比)为18.0%。结合资料分析,在43.9℃~377.9℃范围中,KMnO4分解反应主要以____(填“a”或“b”)为主。