��Ŀ����
����Ŀ�����ſ�ѧ�ķ�չ������Դ�Ŀ�������ȡ��ͻ�ơ��廪��ѧ�о���Ա�ɹ����Ƴ�һ��������ά�������ɽ�������̼ת����Һ��ȼ�ϼ״�������ʾ��ͼ����ͼ��ͼ�е���ǡ ����ȫ��Ӧ����ʾ���������ʾ��ͼ�ش��������⡣
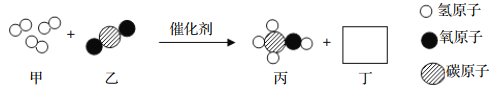
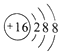
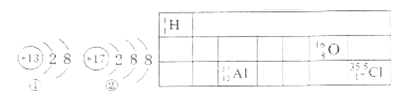
��1�����Ļ�ѧʽΪ______���÷�Ӧ�Ļ�ѧ����ʽΪ______��
��2������˵����ȷ����______����д��ĸ��ţ���
A����Ӧǰ��ԭ����Ŀ�����ı�
B���÷�Ӧ���ڸ��ֽⷴӦ
C�����ǵ��ʣ��ҡ���������Ϊ������
D���÷�Ӧ������������һ�������¿���ת��Ϊ�л���
���𰸡� H2O�� 3H2+CO2![]() CH4O+H2O (��3H2+CO2
CH4O+H2O (��3H2+CO2![]() CH3OH+H2O)�� CD
CH3OH+H2O)�� CD
����������1�����ݷ�Ӧ����ʾ��ͼ�������غ㶨�ɷ����������2�����ݷ�Ӧ�Ļ�ѧ����ʽ�����������Ŀ��Ϣ�������غ㶨�ɿ�֪���÷�Ӧ�ķ���ʽΪ��������̼�������ڴ��������·�Ӧ���ɼ״���ˮ�Ļ�ѧ����ʽΪ3H2+CO2![]() CH4O+H2O (��3H2+CO2
CH4O+H2O (��3H2+CO2![]() CH3OH+H2O)����1����������Ӧ��֪�����Ļ�ѧʽΪH2O���÷�Ӧ�Ļ�ѧ����ʽΪ3H2+CO2
CH3OH+H2O)����1����������Ӧ��֪�����Ļ�ѧʽΪH2O���÷�Ӧ�Ļ�ѧ����ʽΪ3H2+CO2![]() CH4O+H2O (��3H2+CO2
CH4O+H2O (��3H2+CO2![]() CH3OH+H2O)����2��A����������Ӧ��֪����ѧ��Ӧǰ��ԭ����Ŀû�з����ı䣬����B����������Ӧ��֪���÷�Ӧ�����ڸ��ֽⷴӦ������C�������Ĺ��ɿ�֪�����ǵ��ʣ��ҡ���������Ϊ�������ȷ��D����������Ӧ���ʵı仯��֪���÷�Ӧ�������������ת��Ϊ�л����ȷ����ѡCD��
CH3OH+H2O)����2��A����������Ӧ��֪����ѧ��Ӧǰ��ԭ����Ŀû�з����ı䣬����B����������Ӧ��֪���÷�Ӧ�����ڸ��ֽⷴӦ������C�������Ĺ��ɿ�֪�����ǵ��ʣ��ҡ���������Ϊ�������ȷ��D����������Ӧ���ʵı仯��֪���÷�Ӧ�������������ת��Ϊ�л����ȷ����ѡCD��

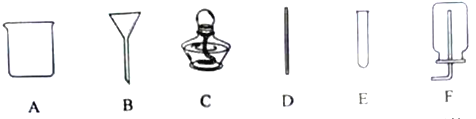
����Ŀ���Ա�ʵ����ʵ��̽������Ҫ���������жԱ�ʵ�������ʵ����Ӧʵ��Ŀ�ĵ���
ѡ�� | ʵ��Ŀ�� | ʵ����� | ѡ�� | ʵ��Ŀ�� | ʵ����� |
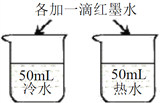
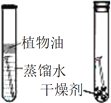
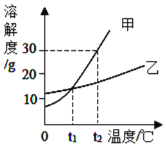
A | ̽���¶ȶԷ����˶�������Ӱ�� |
| B | ̽��ˮ��������ʴ��Ӱ�� |
|
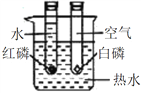
C | ̽��������ȼ�յı�Ҫ���� |
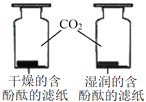
| D | ̽��CO2��ˮ������Ӧ |
|
A. A B. B C. C D. D
����Ŀ����������ͭ�dz��������ֽ�����ͬѧ�Ƿ��������е�����ͭ��Ʒ����һ�㲻�÷��⣬������Ʒһ����Ҫ���������
��������⡿���Dz�����Ϊ��������ͭ���ֽ��������Ļ����ǿ�أ�
��ʵ��̽����ͬѧ�Ƕ������ֽ����Ļ��˳��չ����̽�����������̽������д�ո�
����ϸ��ͬ����˿����˿��ͭ˿�ֱ���������ͬ��������������Ҳ��ͬ��ϡ�����У�
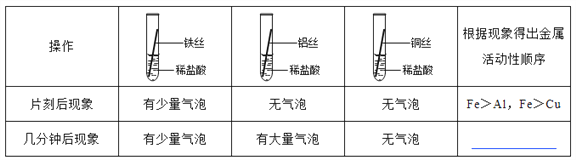
__________________
�����۽�����Ϊʲôͬһ��ʵ��ó������ֽ����أ�ͬѧ�Ǵ���������ʲ�����������ϣ���������˿��ϡ�����ж�ʱ���������ݣ�����Ϊ���������ܵ�����Ĥ���������ᷴӦ��
����˼���ۡ�����������ʵ��ʱ�轫�������д�ĥ����ĥ��Ŀ����__________________________��
�������ᷴӦ�ķ���ʽ��_________________________________________________��
��ʵ����֤��Ϊ�˽�һ��ȷ����������ͭ�����ֽ����Ļ��˳��ͬѧ���ֽ�������ϸ��ͬ�ġ� ��ĥ������˿�ֱ������������Һ������ͭ��Һ�У�
���� |
|
| ��������ó��������˳�� |
���� | ���������� | ______________________ | Al��Fe��Cu |
д����������ͭ��Һ��Ӧ�Ļ�ѧ����ʽ______________________________________________��
����չǨ�ơ���ֻ��һ֧ʢ������ϡ������Թܣ�ֻ��������Ž���˿�IJ���˳��(�������ᷴӦ��Ҫһ�ν�����������)��Ҳ��֤����������ͭ�����ֽ����Ļ��˳����˿�IJ���˳��Ϊ________________________________________________��