题目内容
【题目】碘化钾(KI)是白色固体,保存不当会被氧化为单质碘(I2)而泛黄变质。
化学小组查得以下资料:
I.对于碘化钾变质的原理,有两种不同的反应:
甲:4KI+O2+2CO2=2K2CO3+2I2 乙:4KI+O2+2H2O=4KOH+2I2
II.KOH与NaOH的化学性质相似。
II.K2CO3与稀疏酸的反应与实验室中制取二氧化碳反应原理类似。为探究碘化钾变质原理的合理性,开展以下实验。
[实验过程]
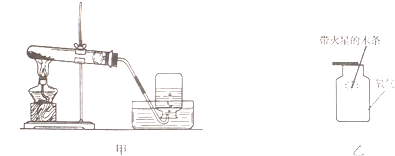
[实验1]取适量碘化钾固体暴露于空气小一段时间,观察到固体泛黄。往泛黄的固体中加入足量稀硫酸,产生无色无味的气体,通入澄清石灰水中,澄清石灰水变浑浊。(1)化学小组认为:据此现象,还不能得出“反应甲是造成碘化钾变质的原因”的结论,因为有可能是反应乙生成的KOH继续与空气中的二氧化碳反应,写出该反应的化学方程式__________。
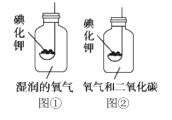
[实验2]按图①所示装置进行实验 ,数日后,观察到碘化钾固体无泛黄现象。
(2)据此现象,可得出的结论是__________
[实验3]按图②所示装置进行实验,数日后,观察到碘化钾固体无泛黄现象。
查阅文献获知,常温下某些气体和固体反应须在潮湿环境中进行。化学小组图①图②据此改进实验,很快观察到固体泛黄的现象。
(3)简述化学小组改进实验的具体措施:__________。
(4)根据上述实验,化学小组得出结论:碘化钾固体泛黄变质是碘化钾与______共同作用的结果。
【答案】2KOH+CO2=K2CO3+H2O 乙不是造成KI变质的原因 往图2所示的装置中加一些水,并塞紧橡胶塞 O2、H2O、CO2
【解析】
(1)KOH与空气中的二氧化碳反应生成碳酸钾和水,方程式故填2KOH+CO2=K2CO3+H2O;
(2)按图①所示装置进行实验 ,数日后,观察到碘化钾固体无泛黄现象,说明水和氧气不是碘化钾变质的原因,故填乙不是碘化钾变质的原因;
(3)根据查阅资料以及实验3,在图2所示的装置中加一些水,使碘化钾在潮湿的环境中和二氧化碳、氧气接触,观察实验,改进措施故填往图2所示的装置中加一些水,并塞紧橡胶塞;
(4)根据上述实验,可知碘化钾固体泛黄变质是碘化钾与水、氧气、二氧化碳共同作用的结果,故填O2、H2O、CO2。