题目内容
【题目】化学实验是学习化学的基础,请根据如图回答问题:
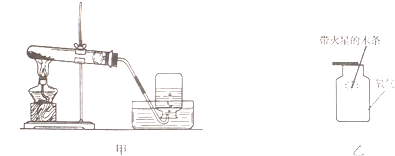
(1)如图甲是实验室制取氧气的装置,用来加热的仪器名称是 ,该反应的化学方程式是 ;为防止水倒流,实验结束时应进行的操作为 ,图中的收集装置还可以收集的气体有 (填写一种).
(2)如图乙将带火星的木条伸到盛有氧气的集气瓶中,可观察到的现象是 ,说明氧气 .
【答案】(1)酒精灯;2KMnO4![]() K2MnO4+MnO2+O2↑;先移导管,后熄灭酒精灯;氢气(或甲烷、一氧化碳);
K2MnO4+MnO2+O2↑;先移导管,后熄灭酒精灯;氢气(或甲烷、一氧化碳);
(2)带火星的木条复燃;能够支持燃烧.
【解析】
试题(1)用来加热的仪器名称是酒精灯;该装置是在试管口有一团棉花,故是加热高锰酸钾制取氧气,产生锰酸钾、二氧化锰和氧气,反应的方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑;实验结束后,应先移导管,后熄灯,否则试管内温度降低,水会倒流入试管使试管炸裂;图中的收集装置是排水集气法,适合难溶于水的气体的收集,因此还可以收集的气体有氢气、甲烷、一氧化碳等
K2MnO4+MnO2+O2↑;实验结束后,应先移导管,后熄灯,否则试管内温度降低,水会倒流入试管使试管炸裂;图中的收集装置是排水集气法,适合难溶于水的气体的收集,因此还可以收集的气体有氢气、甲烷、一氧化碳等
(2)因为氧气具有支持燃烧的性质,故将带火星的木条伸入瓶中,木条复燃

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某小组同学在用过氧化氢溶液与![]() 制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。对此,它们进行了如下探究:
制取氧气的过程中,发现反应的速率很慢,产生的气泡很少。对此,它们进行了如下探究:
(猜想与假设)
①速率慢、气泡少可能与过氧化氢溶液的浓度有关。
②速率慢、气泡少可能与![]() 的质量有关。
的质量有关。
(进行实验)
根据图甲进行如下实验。
实验1:用26mg![]() 与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
与5mL不同浓度过氧化氢溶液进行实验,压强变化如乙图1。
实验2:用5mL 1.5%过氧化氢溶液与不同质量![]() 进行实验,压强变化如乙图2。
进行实验,压强变化如乙图2。
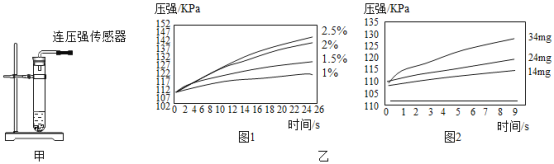
(解释与结论)
(1)实验1得到的结论是______,实验2的目的是______。欲得出“![]() 能加快过氧化氢的分解”这一结论,需要对比______。(简要的写出实验设想)
能加快过氧化氢的分解”这一结论,需要对比______。(简要的写出实验设想)
(2)小组同学查阅资料得知:多种物质能催化过氧化氢的分解。
(实验探究)
实验证明,![]() 溶液也能显著加快过氧化氢的分解,
溶液也能显著加快过氧化氢的分解,![]() 溶液主要含有三种粒子(
溶液主要含有三种粒子(![]() ),稀硫酸中含有三种粒子(
),稀硫酸中含有三种粒子(![]() )为了进一步探究
)为了进一步探究![]() 溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计:
溶液中哪种粒子能起催化作用,小组同学作了以下分析和设计:
①小组同学认为最不可能的是![]() ,他们的理由是______。
,他们的理由是______。
②要说明另外的两种粒子是否起到催化作用,小组同学设计了如下实验,完成探究活动。
实验步骤 | 实验现象 | 结论 |
a.取一支试管加入5mL 5%过氧化氢溶液,然后加入2-3滴稀硫酸 | 溶液中几乎没有气泡放出 | 验证明,起催化作用的是______。 |
b.另取一支试管加入5mL 5%过氧化氢溶液,然后加入2-3滴硫酸铜溶液 | 溶液中有大量气泡放出 |
(3)(反思与评价)
小组同学在进行实验1和2制取氧气过程中,发现反应的速度很慢,产生的气泡很少的原因可能是______、______。
(4)利用图甲装置不能探究“温度对过氧化氢分解速率”的影响,其理由是______。