题目内容
【题目】某工业废液中含有CuSO4、ZnSO4、FeSO4,如果将废液直接排放就会造成水污染.于是几位同学设计实验处理废液,回收工业重要原料硫酸锌和有关金属.实验过程如下:

请回答:
(1)操作①的名称是_____.需要的玻璃仪器有烧杯、________ 、玻璃棒。
(2)步骤①中加入过量M的化学式_________.请写出工业上用赤铁矿(主要成分为Fe2O3)炼铁的化学方程式____________.
(3)若加入一定量M(不考虑上述实验过程中后续实验现象和结论),则滤液A中一定含有的溶质的化学式是_________
【答案】过滤 漏斗 Zn Fe2O3 + 3CO![]() 2Fe + 3CO2 ZnSO4
2Fe + 3CO2 ZnSO4
【解析】
(1)操作①能固液分开,名称是过滤;需要的玻璃仪器除了烧杯、玻璃棒外,还需要漏斗;
(2)由上述分析可知,步骤①中加入过量的M是锌,化学式是:Zn;工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(3)若加入一定量M是锌,则滤液A中一定含有的溶质的化学式是:ZnSO4。

 名校课堂系列答案
名校课堂系列答案【题目】现在多数家庭使用天然气或液化石油气。液化石油气主要成分是丙烷和丁烷。已知:无水硫酸铜CuSO4遇到水由白色变为蓝色,常用于检验水的存在;浓硫酸具有强吸水性;氢氧化钠溶液能吸收二氧化碳。
(1)写化学式:甲烷CH4、乙烷C2H6、丙烷C3H8、丁烷_____、戊烷C5H12
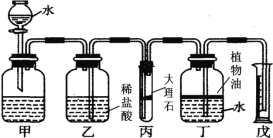
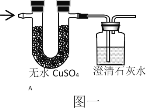
(2)写出丙烷C3H8完全燃烧的化学方程式_____;将丙烷C3H8完全燃烧产物通入“图一”装置,则无水硫酸铜由白色变为____色,澄清石灰水变浑浊的化学反应方程式_____。
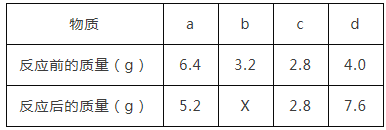
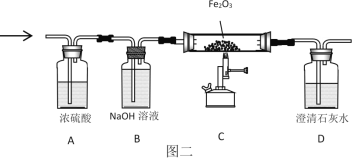
(3)将13.2g丙烷C3H8与38.4g氧气O2充分反应后生成物依次通过“图二”装置;认真阅读下表,回答相关问题:
物质 质量 /g | 丙烷C3H8 | 氧气O2 | 装置A | 装置B | X |
反应前 | 13.2 | 38.4 | 508.2 | 485.4 | 0 |
反应后 | 0 | 0 | 529.8 | 498.6 | a |
①a=_____;求物质X的化学式(写出计算过程)
②写出13.2g丙烷C3H8与38.4g氧气O2充分反应的化学方程式_____。
③装置C中的现象是_____;化学反应方程式是_____。由上可知“图三”装置有一处明显不足_____。
④判断CO2是否被装置B完全吸收的方法:在装置B、C之间增加装有澄清石灰水的洗气瓶,若澄清石灰水_____,则CO2被完全吸收。
⑤若增加氧气的量,则X与H2O的化学计量数之比将_____(填“变大”、“不变”或“变小”)。