��Ŀ����
����Ŀ����ͼ��ѡ��4��װ������ȡ�ϴ�����CO2���塣
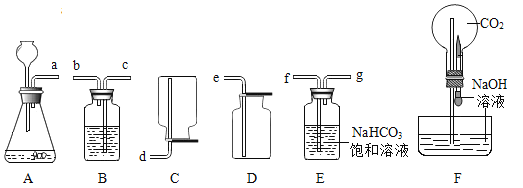
��1����ȷ�Ľӿ�˳�����������Ϊ�� a��_____��B��ʢ�ŵ�Һ����_____��
��2��ָ����ѡװ����һ�����ԵĴ�����_____��
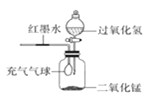
��3����ͼ�е�Fװ�ÿ�������ʮ����Ȥ�ġ���ѧ��Ȫ��������ͷ�ι��е�NaOH��Һ����Բ����ƿʱ���ܿ쿴�������ܶ��˲�������Ȫ������������Ȫ�������ԭ����_____��������ƿ�ڵ�CO2�����������������е�_____������ĸ��ţ��Կɲ�������Ȫ������
A SO2
B H2
C CO
D HCl
���𰸡�fgcbe Ũ���� ����©�����¶�û������Һ������ ������̼������������Һ��Ӧʹƿ��ѹǿ��С AD
��������
��1����ȡ�����Ķ�����̼���壬���Ȱ�װ���巢��װ�ã������ӳ���װ�ã�����װ�ã���������ռ�װ�ã�������������˳����AEBF���� a��fgcbe������fgcbe��
װ��B�����������壬���е�Һ̬�������Ũ���ᣬ����Ũ���ᡣ
��2��ͼ��Aװ���д��ô����dz���©�����¶�û������Һ�����£���������ɵ������س���©����ɢ�������У������©�����¶�û������Һ�����¡�
��3����������Ȫ�������ԭ���Ƕ�����̼���������Ʒ�Ӧ��ʹƿ�ڵ�ѹǿ��С�ҵ��ڴ���ѹ������ѹ��ˮ���е�ˮѹ��ƿ���γ���Ȫ�����������̼���������Ʒ�Ӧʹƿ�ڵ�ѹǿ��С��
A SO2�����������Ʒ�Ӧ����ʹƿ��ѹǿ��С�γ���Ȫ��ѡ����ȷ��
B H2�������������Ʒ�Ӧ��ƿ��ѹǿ���䣬�����γ���Ȫ��ѡ�����
C CO�������������Ʒ�Ӧ��ƿ��ѹǿ���䣬�����γ���Ȫ��ѡ�����
D HCl�����������Ʒ�Ӧ����HCl������ˮ����ʹƿ��ѹǿ��С�γ���Ȫ��ѡ����ȷ������AD��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ�������仯����������������Ӧ�÷dz��㷺��
��һ�������ϵ��й�֪ʶ

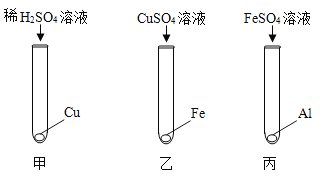
��1������ʹ�ý����Ⱥ���������ͭ������������ʱ����ֱ�������ſ�ʼ����ʹ�������ϡ���Ҳ��ӳ��Cu��Fe�� Al���ֽ����Ļ����ǿ������˳����_______________��
��2��������������˾�ϣ���ͼ���IJ��ϣ�������������������������Ҫ��________________��
��3���ҹ�C919���Ϳͻ�ȥ�꾪�����࣬�ͻ��ϴ��ģʹ��̼��ά���ϲ��ϡ���﮺Ͻ����ѺϽ������մɵ��Ƚ����ϣ����в��漰���IJ�����_________��ѡ����ţ���
A �Ͻ�
B ���ǽ�������
C �ϳɲ���
D ���ϲ���
��4������ʯ�г�������������FeS2���ȡ���ҵ���û�������ȡ���������������������������ԭ����:��ұ���в���SO2��Ⱦ��������______________��
��������ȡ��ʽ������
��ʽ��������-�ַ�ˮ�������������᳧�ķ�������Ҫ�ɷ�Ϊ�������������FeS��SiO2���Ʊ���ʽ����������[Fe4��OH��2��SO4��5��6H2O]��Ҫ��������:

��1������Ӧ��ĥ�ɷ�ĩ��Ŀ����_____��
��2��������������������H2S����Ļ�ѧ����ʽΪ________
��3�����˺�ϴ�ӣ�֤��������ϴ���ķ�����_______��
��4����ת����������Ӧ�Ļ�ѧ����ʽΪ_______���÷�Ӧ�¶Ȳ��˹��ߵ�ԭ����________��
��������ʽ������������ȷֽ�ʵ��
��ȤС���ȡ�˾�����Ʒ25.38g���ڿ�����Ա��ָ��������ͼװ�ý����ȷֽ�ʵ�顣
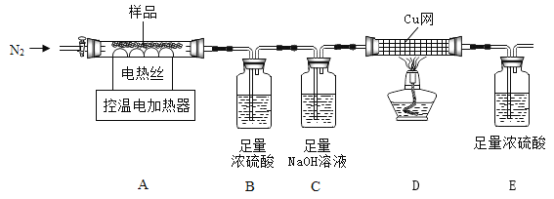
[��������]�ټ�ʽ���������壨��Է�������Ϊ846��200��C��ȫ�ֽ�����Fe2O3��H2O��Fe2��SO4��3��
��Fe2��SO4��3��500��C��ȫ�ֽ�ΪFe2O3��SO2��SO3��O2��
��Bװ����Ũ����ֻ������SO3��H2O��.
��1��װ���ʵ��װ�ú���Ҫ_________��
��2������ǰ�����о�ͨ��N2,ֹͣ���Ⱥ����ͨN2��Ŀ���Ƿ�ֹ������______��
��3�����Ʋ�ͬ���¶ȶ�A�й�����ȣ����װ��B��C��D�е������仯���±������ʣ������������¶ȵı仯��ͼ��ʾ��

�¶�/C | ���� | 220 | 520 |
Bװ��/g | 200.00 | 203.78 | 207.78 |
Cװ��/g | 200.00 | 200.00 | x |
Dװ��/g | 100.00 | 100.00 | 101.60 |
����ͼ��m1=____________��
�ڱ�����x=_____________��
�۽����յ�ʣ�����������ȵ����ߵ��¶ȣ����ֹ������0.32g���������ٸı䣬д���˹����з�����Ӧ�Ļ�ѧ����ʽ____________��
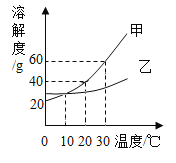
����Ŀ������г���KNO3��NaCl�ڲ�ͬ�¶�ʱ���ܽ�ȣ�
�¶ȣ����� | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
KNO3�ܽ�ȣ�g�� | 13.3 | 20.9 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl�ܽ�ȣ�g�� | 35.7 | 35.8 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
���к�123g KNO3��17.9g NaCl�Ļ���ijͬѧ���������ʵ���ȥKNO3�е�NaCl��
���������м�������ˮ�������ܽ⣻
�ڼ���������Һ��100������������Ũ��������ص��ȱ�����Һ��
�۽���Һ������10�������õ�KNO3���壬���ˣ�������KNO3����ϴ�Ӳ����
��1���ڲ�����У�Ϊȷ��û�о�����������Һ������Ҫ����_____gˮ
��2���ڲ�����У����ɵõ�KNO3����_____g
��3����ȥKNO3������NaCl����Ҫʵ�����̿�����ͼ��ʾ��
![]()
������ȱ�ٵIJ�����_____��
��4��ϴ��ʱ��Ӧѡ������_____��ѡ������ˮ��������ˮ������֤���Ѿ�ϴ�Ӹɾ��ķ�����_____��