��Ŀ����
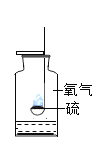
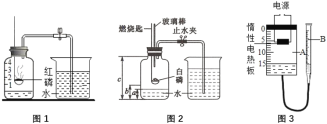
����Ŀ��ͼ1�ǿα��������������������ⶨ����ʵ��װ�á���ʵ��ʹ���У���������ʵ����ƫС�������ԭ�������_________����һ������ij��ѧ̽����ѧϰС��������������������ⶨ����ʵ������˸Ľ���
���������ϣ�
���ͺ������Ԫ����ͬ������ȼ�����������¶���40������������Ҫ240����
�����ʵ�飩
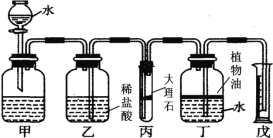
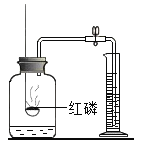
ʵ��װ����ͼ2��ʾ��
��ʵ�鲽�裩
�ٴ�����ȼ����ϣ�������ƿ�Լ���������ʧ��
��Ѹ�ٽ�Ԥ�ȹ��IJ�������������Ӵ����۲쵽����ȼ�ա�
���ڼ���ƿ��װ������a�����ˮ��ȼ�ճ����һ����ף��ھƾ����ϰѲ������¶˼��Ⱥ����̽�����ƿ�ϵ�������������
�ܸ���a��b��c�������ݣ���������������������������
����ͼ2��ʾ�������������________��
������ƿ��ȫ��ȴ�����£���ֹˮ�У���������ƿ��ˮ�����Ϊb����������ƿ�����Ϊc��
��������ʵ����Ϣ���ش������й����⣺
��1����ȷ��ʵ��˳����________������ţ���
��2����ʵ��dz��ɹ�����д��a��b��c��������Ӧ�����һ����ʽ��ϵ__________��
��3��ҩƷ�а�������Ӧ��֤��������Ŀ����__________��
��ʵ����չ��
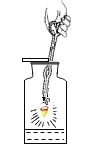
��һ��̽��С���������һ���Ľ�װ�ã���ͼ3��ʾ������A��ԲͲ״�������������ܷ�ǣ����������������Ϊ��λ�Ŀ̶ȣ�B�Ǵ��̶ȵij��ڲ����ܣ���������װ���ԣ�����������ͭ��ƽ���ڶ��Ե��Ȱ��ϣ��ǽ��ܷ�ǡ�ͨ�����ͭ�ۣ���ַ�Ӧ����ȴ��ԭ����״̬������B�ĸ߶�ʹ����A��B�е�Һ�汣����ƽ����¼Һ��̶ȡ���ע��A�����ڹ�̬������ռ��������Բ��ƣ�
��4��д����ʵ���ԭ��__________��д����ط�Ӧ����ʽ����
��5���˸Ľ�װ�öԱȿα��ϵ�ʵ��װ�ã��ŵ���________����һ�����ɣ���
��6�����������У�����B�ĸ߶�ʹ����A��B�е�Һ�汣����ƽ��Ŀ����_________��
���𰸡�װ�������Բ�������ɣ� װ�������� �ݢۢڢ٢ޢ� c+4a=5b ��ƿ��������������� ![]() ����С ȷ�����ݻ��ڵ�ѹǿ��ͬ����Сʵ�����
����С ȷ�����ݻ��ڵ�ѹǿ��ͬ����Сʵ�����
��������
���ײⶨ��������������ʵ���У�ͨ��ˮ���������ó������ĺ�����������ʵ����ƫС��ԭ������ǣ���װ�������Բ��Ӧ���������п������룻�ں��������㣬�������ܺľ�����δ��װ����ȴ�����¾ʹ�ֹˮ�У�ƿ����������������ͣ��ܵ����ڿ���������ˮ������
��1������ͼ2װ�ý���ʵ�飬����Ҫ���ȼ��װ�������ԣ�Ȼ�����ҩƷ����������Ԥ�ȵIJ�������ȼ���ף�����Ӧ��ȫ��װ����ȴ�����£���ֹˮ�У���¼���ݣ�����������ĺ����������ȷ��ʵ��˳��Ӧ���Ǣݢۢڢ٢ޢܣ�����������Ӻ��������װ�������ԣ���֤ʵ��ijɹ���
��2�������ĺ���Լռ���������֮һ����˽��뵽ƿ�ڵ�ˮ�����ҲӦ����ռ�ȷֵ����֮һ���ɴ���![]() ��
��
��3�������������㣬��ƿ�ڵ����������ľ����ᵼ�²���ǽ����ʵ��ƫС��������Ŀ�ľ��ǽ�����������ĵ���
��4���÷�Ӧ���ø�ͭ�ۼ��ȣ�����������ԭ���ǣ�![]() ��
��
��5������ȼ��ʱ������Ũ�Ƚ��͵�ijһ��ʱ�ͻ�Ϩ�����������������ʵ����ͭ�ۻ�һֱ��������Ӧ�����������ľ������Ҳ�������Ⱦ��ŵ��ǣ�����С���Ի�������Ⱦ��
��6��ֻ�е�AB�е�Һ����ƽʱ������ȷ�����ݻ��ڵ�ѹǿ��ͬ�������������ݲ�ȷ��

����Ŀ���±�����������ˮ���ұ��IJ������ݣ���������ˮˮ�ʳ��������Ŀ����ֵ�����֣�
��Ŀ | ��ֵ |
ɫ�� | ������15�ȣ������ó���������ɫ |
���Ƕ� | ������1�ȣ���������²�����5�� |
pH | 6.5��8.5 |
��Ӳ�ȣ���CaCO3�ƣ� | 450mg/L |
�� | 0.2mg/L |
�� | 0.3mg/L |
������ | 250mg/L |
��1���ϱ���������ָ����_____��ѡ��������������Ԫ��������ԭ��������
��2��������Ӳˮ�����ķ�����_____��
��3��ʵ����������ˮ��ͨ��ֽ⣬���������������������ԼΪ_____��
��4��������Ư�۵���Ч�ɷ���Ca(ClO)2��������Ԫ�صĻ��ϼ���_____��
��5��1L�ϸ����������ˮ�У�����CaCO3����Ӳ�ȣ����Ԫ�صĺ���������_____mg/L��
��6���ڳ��õľ�ˮ�ķ����У������̶���ߵ���_____
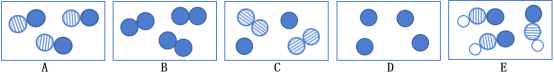
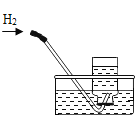
����Ŀ��������ʵָ�������е�ˮ�������û������ˮ����Ҫ���õ��ǣ� ��
ʵ��װ�� |
���ڿ�����ȼ�� |
�ⶨ�����������ĺ��� |
��˿��������ȼ�� |
��ˮ���ռ����� |
���� | ����ƿ�е�ˮ�����շų������� | ��Ͳ�е�ˮ��ͨ��ˮ������仯�ó���������� | ����ƿ�е�ˮ����ȴ�����������ֹ����ƿը�� | ����ƿ�е�ˮ��ˮ�Ƚ�����ƿ�еĿ����ž�������ڹ۲�H2��ʱ�ռ��� |
A.AB.BC.CD.D