题目内容
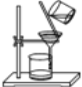
【题目】下图是初中化学课堂中出现的装置,请据图回答:
(1)四个图中均含有同一种仪器,它的名称是_______________.
(2)写出图1中发生反应的化学方程式__________________
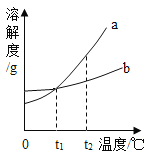
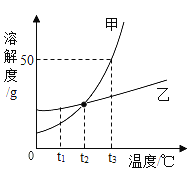
(3)由图2可以得出的实验结论是__________
(4)图3中a试管装有白磷和空气、b试管装有红磷和空气,烧杯中盛有80℃热水,底部有一小块白磷,可以得出“可燃物燃烧需要氧气”的实验对比现象是_______________
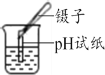
(5)图4实验中铁钉最易生锈的部位是________(填①、②或③)。
【答案】试管 ![]() 水是由氢元素和氧元素组成(或水分子有氢原子和氧原子构成) 试管a中的白磷燃烧,烧杯水中的白磷没有燃烧 ②
水是由氢元素和氧元素组成(或水分子有氢原子和氧原子构成) 试管a中的白磷燃烧,烧杯水中的白磷没有燃烧 ②
【解析】
(1)四个图中均含有同一种仪器,它的名称是:试管;
(2)图1中试管口有棉花,是高锰酸钾加热产生锰酸钾、二氧化锰和氧气,发生反应的化学方程式![]() ;
;
(3)图2中电解水产生氢气和氧气,可以得出的实验结论是:水是由氢元素和氧元素组成;
(4)图3中a试管装有白磷和空气、b试管装有红磷和空气,烧杯中盛有80℃热水,底部有一小块白磷,可以得出“可燃物燃烧需要氧气”的实验对比现象是:试管a中的白磷燃烧,烧杯水中的白磷没有燃烧;
(5)图4实验中铁钉同时和水和空气接触最易生锈,部位是:②。

 寒假学与练系列答案
寒假学与练系列答案【题目】请回答下列问题:
(1)铝热反应是焊接铁路上钢轨的反应原理:即在高温下铝与氧化铁发生反应生成氧化铝和铁,写出该反应的化学方程式_____该反应属于_____反应(填基本类型)
(2)下面是部分金属的部分物理性质:
物理性质 | 物理性质比较 |
导电性 |
|
密度 |
|
由上表可知:用铝作高空电缆是因为_____、_____。
(3)认真观察分析比较下列几个反应及现象:
A “真金不怕火炼”金在高温下也不与氧气发生反应。Au+O2![]() (不反应)
(不反应)
B 金属镁在空气中燃烧,发出耀眼的强光,放出大量的热量。2Mg+O2![]() 2MgO
2MgO
C 铜在加热条件下与氧气发生反应,在表面变黑。2Cu+O2![]() 2CuO
2CuO
D 铝在空气中与氧气发生反应,在表面生成一层致密的氧化膜。2Al+3O2=2Al2O3
从上述实验事实可以看出,四种金属的活动性顺序是_____。
【题目】为探究酸的化学性质,某化学小组利用盐酸进行了如下实验操作,请回答:
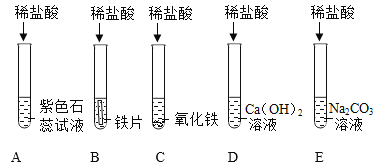
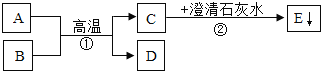
(1)写出C中反应的化学方程式___________________。
(2)装置B中的反应现象:首先观察到__________________,随后观察到___________________,发生反应的化学方程式是___________________。
(3)将反应后D.E试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行如下探究:
(提出向题)滤液中溶质的成分是什么?
(作出猜想)
猜想一:NaCl
猜想二:NaC1和CaCl2
猜想三:NaC1、CaCl2和Na2CO3
猜想四:______________(填化学式)
(进行讨论)经过讨论,同学们一致认为猜想____________________是错误的。
(设计实验)请完成实验报告。
实验步骤 | 实验现象 | 实验结论 |
取少量滤液于试管中,滴加适量的碳酸钠溶液 | 无明显现象 | 猜想二不成立 |
取少量滤液于试管中,滴加氯化钡溶液 | ________________ | 猜想四成立 |
(4)某工厂化验室用10%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40g,洗涤后的溶液呈中性。计算这些石油产品中含硫酸的质量是多少?___________