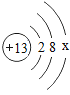题目内容
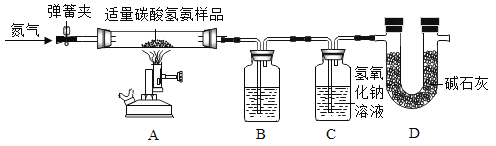
【题目】已知A、B为两种黑色粉末,D为红色单质。A、B、C、D、E五种物质之间的转化关系如下图所示。请回答:
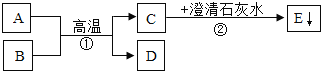
(1)C的化学式为_____;
(2)标出A中金属元素化合价____;
(3)反应①的化学方程式为_____;该反应的基本类型是_____。
(4)反应②的化学方程式为_______。
【答案】CO2 ![]()
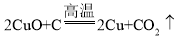 置换反应
置换反应 ![]()
【解析】
A、B为两种黑色粉末,D为红色单质,A、B在高温的条件下反应生成C和D,氧化铜和碳都是黑色,且氧化铜能与碳在高温的条件下反应生成铜和二氧化碳,铜为红色,可推出A、B为氧化铜和碳,C为二氧化碳,D为铜;二氧化碳可与氢氧化钙反应生成碳酸钙和水,故E为碳酸钙。
(1)C为二氧化碳,化学式为:CO2;
(2)标出A中金属元素化合价,则A为氧化铜,铜通常为+2价,元素化合价的表示方法是在化学式该元素的上方用正负号和数字表示,正负号标在数字前面,故标出A中金属元素化合价为:![]() ;
;
(3)反应①为氧化铜和碳在高温的条件下反应生成铜和二氧化碳,该反应的化学方程式为: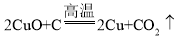 ,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;
,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;
(4)反应②为二氧化碳与氢氧化钙反应生成碳酸钙和水,该反应的化学方程式为:![]() 。
。

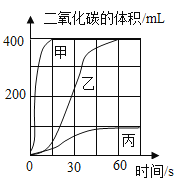
【题目】实验室制备并收集二氧化碳,按下表进行实验。取等质量的同种大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如图所示。下列说法错误的是
实验编号 | 药品 |
Ⅰ | 块状大理石、10% H2 SO4溶液 |
Ⅱ | 块状大理石、7% HCl溶液 |
Ⅲ | 大理石粉末、7% HCl溶液 |
A.实验Ⅲ对应的左图变化曲线为甲
B.实验II和Ⅲ对比,说明影响反应速率的因素是固体的颗粒大小
C.实验I和Ⅱ对比,说明影响反应速率的因素是酸的浓度
D.实验Ⅱ和Ⅲ完全反应后,产生二氧化碳的质量是相等的