题目内容
【题目】据图回答下列问题:

(1)图1为实验室用高锰酸钾制取氧气的装置。
①实验中反应的化学方程式为________。
②氧气可用排水法收集的原因是________。
(2)利用图2所示装置探究可燃物燃烧的条件(热水温度高于白磷着火点)。
①对比铜片上白磷燃烧和红磷不燃烧的现象,说明可燃物燃烧的条件之一是________。
②能说明可燃物燃烧需要与氧气接触的现象是________。
③烧杯中热水所起的作用是________。
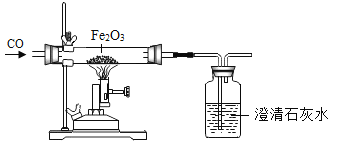
(3)利用图3装置进行下列实验(烧杯中放着一支燃着的蜡烛),打开K。
①广口瓶中发生反应的化学方程式是________。
②观察到蜡烛_______,说明影响燃烧剧烈程度因素之一是______。
【答案】2KMnO4 ![]() K2MnO4 + MnO2 + O2↑ 氧气不易溶于水且不与水反应 温度达到可燃物的着火点 水中的白磷不燃烧,铜片上的白磷燃烧 加热、隔绝氧气 2H2O2
K2MnO4 + MnO2 + O2↑ 氧气不易溶于水且不与水反应 温度达到可燃物的着火点 水中的白磷不燃烧,铜片上的白磷燃烧 加热、隔绝氧气 2H2O2![]() 2H2O + O2↑ 燃烧更旺 氧气浓度
2H2O + O2↑ 燃烧更旺 氧气浓度
【解析】
(1)①高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,要注意配平;
②氧气不易溶于水且不与水反应,因此能用排水法收集;
故答案为:①2KMnO4![]() K2MnO4+MnO2+O2↑;②氧气不易溶于水且不与水反应;
K2MnO4+MnO2+O2↑;②氧气不易溶于水且不与水反应;
(2)①对比铜片上白磷燃烧和红磷不燃烧的现象,因为温度没有达到红磷的着火点,说明可燃物燃烧的条件之一是:温度达到可燃物的着火点;
②能说明可燃物燃烧需要与氧气接触的现象是:相同条件下,水中的白磷不燃烧,铜片上的白磷燃烧;
③烧杯中热水所起的作用是:加热、隔绝氧气。
故答案为:①温度达到可燃物的着火点;②水中的白磷不燃烧,铜片上的白磷燃烧;③加热、隔绝氧气;
(3)①广口瓶中发生过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;②观察到蜡烛燃烧更旺,说明影响燃烧剧烈程度因素之一是:氧气浓度。
故答案为:①2H2O2![]() 2H2O+O2↑;②燃烧更旺;氧气浓度。
2H2O+O2↑;②燃烧更旺;氧气浓度。

 阅读快车系列答案
阅读快车系列答案【题目】野外探险,可以利用供氧剂过氧化钠(Na2O2)与CO2反应制取O2, 化学反应方程式为:![]() 。
。
(1) Na2O2中O元素的化合价是_______________。
(2)某兴趣小组的同学查阅资料,了解到二氧化硫(SO2)性质与CO2类似,可以与水反应生成亚硫酸(H2SO3),也可以与生石灰反应生成亚硫酸钙(CaSO3),还可以与氢氧化钠反应生成亚硫酸钠(Na2SO3)。
(提出问题)二氧化硫(SO2)与过氧化钠(Na2O2)反应,是否与CO2的完全一致?
(查阅资料)
I.少量二氧化硫(SO2)通入澄清石灰水中,也可以看到溶液变为混浊。写出溶液变为浑浊所发生的化学反应方程式_______________。
Ⅱ.亚硫酸钠(Na2SO3)固体和盐酸反 应会放出二氧化硫(SO2);
Ⅲ.亚硫酸钡(BaSO3)固体不溶于水,但可溶于盐酸放出二氧化硫(SO2)。
(提出猜想)二氧化硫(SO2)与过氧化钠(Na2O2)反应,若过氧化钠(Na2O2)完全反应,生成的固体产物;
猜想一:可能只有Na2SO3;
猜想二:可能只有Na2SO4;
猜想三:可能___________________
(设计实验)
实验步骤 | 实验现象 | 解释或结论 |
①取少量固体产物于烧杯,加入蒸馏水,搅拌溶解。 | 固体完全溶解。 | 钠盐均可溶于水。 |
②取少量①中所得溶液于试管,加入盐酸溶液。 | 有气体放出。 | 说明猜想_________(填“一”或“二”或“三”)是错误的。 |
③另取少量①中所得溶液于试管,加入适量BaCl2溶液, 过滤。 | 有沉淀生成。 | 生成的沉淀可能是__________(填化学式)。 |
④取③中得沉淀,加入足量的_________溶液。 | 有气体放出,沉淀部分溶解。 | 说明猜想三成立。 |
(实验结论)
猜想三成立。请写出④中放出气体所发生的化学反应方程式_______________。
(交流讨论)实验结束后,同学们一起讨论, 二氧化硫(SO2)与过氧化钠(Na2O2)反应生成硫酸钠是什么原理?他们带着这个问题去请教老师:老师告诉他们,二氧化硫(SO2)与过氧化钠(Na2O2)反应生成硫酸钠,是氧化还原反应。在氧化还原反应中,有元素化合价升高,必定有元素化合价降低。硫酸钠的生成,有两种可能:
a.生成的亚硫酸钠(Na2SO3)被O2氧化所得,发生的化学反应方程式为_______________。
b.过氧化钠(Na2O2)直接将二氧化硫(SO2)氧化所得。