题目内容
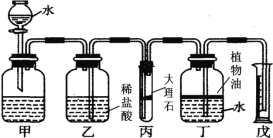
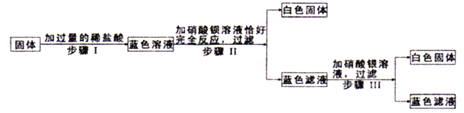
【题目】氯化钙是多用途的干燥剂和建筑防冻剂。实验室里用石灰石和盐酸制备二氧化碳的含酸废液(含有MgCl2、CuCl2等)通过以下途径制得无水氯化钙。
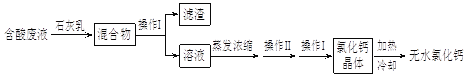
(1)操作I的名称为_______,滤渣的化学成分有_____________。
(2)石灰乳的作用是:① 中和废液中的酸;②___________,写出作用②的其中一个反应方程式___________。
【答案】过滤 Mg(OH)2、Cu(OH)2 ②使废液中的镁、铁充分沉淀 MgCl2+ Ca(OH)2=Mg(OH)2↓+CaCl2 或CuCl2 +Ca(OH)2=Cu(OH)2↓+CaCl2
【解析】
氯化镁和氢氧化钙生成氢氧化镁和氯化钙或氯化铜和氢氧化钙反应生成氢氧化钙和氯化钙.
(1)操作I是将固体和液体分离,名称为过滤,石灰石和盐酸制备二氧化碳的含酸废液(含有MgCl2、CuCl2等),甲石灰乳生成氢氧化镁和氢氧化铜,故滤渣的化学成分有Mg(OH)2、Cu (OH)2。
(2)石灰乳的作用是:① 中和废液中的酸;②使废液中的镁、铁充分沉淀,作用②的反应是氯化镁和氢氧化钙生成氢氧化镁和氯化钙或氯化铜和氢氧化钙反应生成氢氧化钙和氯化钙,反应的化学方程式为MgCl2+ Ca(OH)2= Mg(OH)2↓+CaCl2 或CuCl2 + Ca(OH)2= Cu (OH)2↓+CaCl2。

【题目】下表是生活饮用水国家标准的部分内容,生活饮用水水质常规检验项目及限值(部分)
项目 | 限值 |
色度 | 不超过15度,并不得呈现其他异色 |
浑浊度 | 不超过1度,特殊情况下不超过5度 |
pH | 6.5﹣8.5 |
总硬度(以CaCO3计) | 450mg/L |
铝 | 0.2mg/L |
铁 | 0.3mg/L |
硫酸盐 | 250mg/L |
(1)上表中“铝”指的是_____(选填“单质”、“元素”或“原子”);
(2)生活中硬水软化的方法是_____;
(3)实验室用上述水样通电分解,产生氢气和氧气的体积比约为_____;
(4)消毒剂漂白粉的有效成分是Ca(ClO)2,其中氯元素的化合价是_____;
(5)1L合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量不超过_____mg/L.
(6)在常用的净水的方法中,净化程度最高的是_____
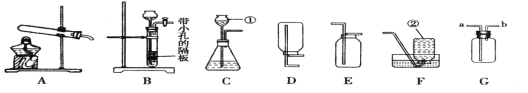
【题目】对下列实指定容器中的水,其解释没有体现水的主要作用的是( )
实验装置 |
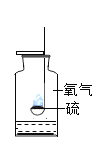
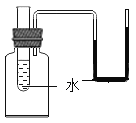
硫在空气中燃烧 |
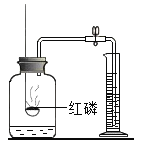
测定空气中氧气的含量 |
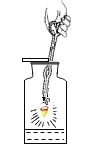
铁丝在氧气中燃烧 |
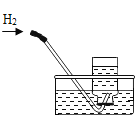
排水法收集氢气 |
解释 | 集气瓶中的水:吸收放出的热量 | 量筒中的水:通过水的体积变化得出氧气的体积 | 集气瓶中的水:冷却溅落熔融物,防止集气瓶炸裂 | 集气瓶中的水:水先将集气瓶中的空气排净,后便于观察H2何时收集满 |
A.AB.BC.CD.D