题目内容
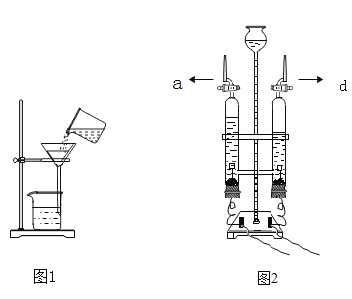
【题目】根据下图回答问题:
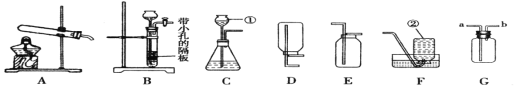
(1)写出图中标号仪器名称:①________;②_______
(2)实验室用A制取并收集干燥的氧气应选用的收集装置是______(填序号,下同),反应的文字表达式为_____。检查装置气密性时,除了用手紧握的方法外,还可以采用的方法是____,若用G装置收集氧气,气体从____(选填“a”或“b”)端导管通入,验满的方法是_____。
(3)实验室可用氧化钙固体与浓氨水在常温下混合制取少量氨气,应选择的发生装置是_____;
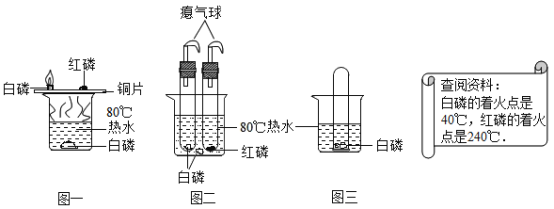
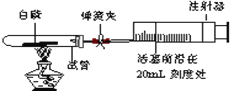
(4)做硫在氧气中燃烧实验,燃烧结束后取出燃烧匙,立即用玻璃片盖住瓶口并振荡,若将集气瓶倒转,发现玻璃片被“吸住”而不掉下来(如甲图),其原因是________;
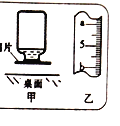
(5)上面实验为了防止二氧化硫污染空气,用l0mL量筒取6mL氢氧化钠溶液,读数时量筒内的液体凹液面最低处应与乙图_____处(填“a"或“b”)刻度线保持水平
(6)现有a、b两份质量相等的固体氯酸钾,a加入少量二氧化锰,b是纯净的氯酸钾,将a、b放入两支试管中同时加加热.放出氧气的质量和反应时间的关系图象正确的是(______)
A 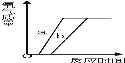 B
B 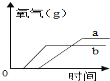
C 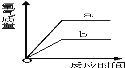 D
D 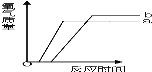
【答案】长颈漏斗 集气瓶 E 氯酸钾![]() 氯化钾+氧气 酒精灯微热或热毛巾包住 a 把带火星(或燃烧)木条放在b处,木条复燃(或燃烧更旺)则收集满 B或C 硫燃烧消耗氧气,生成的二氧化硫又被水吸收,使瓶内压强减小 a A
氯化钾+氧气 酒精灯微热或热毛巾包住 a 把带火星(或燃烧)木条放在b处,木条复燃(或燃烧更旺)则收集满 B或C 硫燃烧消耗氧气,生成的二氧化硫又被水吸收,使瓶内压强减小 a A
【解析】
(1)氧气①是长颈漏斗,仪器②是集气瓶,故填:长颈漏斗;集气瓶;
(2)氧气密度大于空气,收集干燥的氧气应用向上排空气法,装置A是固固加热型装置,试管口没有棉花,是用氯酸钾和二氧化锰加热制取氧气,反应的文字表达式为:氯酸钾![]() 氯化钾+氧气;检查装置气密性时,除了用手紧握的方法外,还可以采用的方法是酒精灯微热或热毛巾包住试管;氧气密度大于空气,若用G装置收集氧气,气体从a端导管通入,验满的方法是把带火星(或燃烧)木条放在b处,木条复燃(或燃烧更旺)则收集满。
氯化钾+氧气;检查装置气密性时,除了用手紧握的方法外,还可以采用的方法是酒精灯微热或热毛巾包住试管;氧气密度大于空气,若用G装置收集氧气,气体从a端导管通入,验满的方法是把带火星(或燃烧)木条放在b处,木条复燃(或燃烧更旺)则收集满。
故填:E;氯酸钾![]() 氯化钾+氧气;酒精灯微热或热毛巾包住试管;a;把带火星(或燃烧)木条放在b处,木条复燃(或燃烧更旺)则收集满;
氯化钾+氧气;酒精灯微热或热毛巾包住试管;a;把带火星(或燃烧)木条放在b处,木条复燃(或燃烧更旺)则收集满;
(3)实验室可用氧化钙固体与浓氨水在常温下混合制取少量氨气,发生装置属于固液常温型的BC装置,故填:B或C;
(4)硫燃烧消耗氧气,生成的二氧化硫又被水吸收,使瓶内压强减小,外界大气压将玻璃片“托住”,所以若将集气瓶倒转,发现玻璃片被“吸住”而不掉下来;故填:硫燃烧消耗氧气,生成的二氧化硫又被水吸收,使瓶内压强减小;
(5)用10mL量筒量取6mL氢氧化钠溶液时,6mL刻度线应该在5mL刻度线上方,是a处.故填:a;
(6)a、b两份质量相等的固体氯酸钾,a加入少量二氧化锰, a中生成氧气的速度较快,但最终生成氧气的质量相同,结合图像可知,A符合题意;故填:A。

 名校课堂系列答案
名校课堂系列答案【题目】彩漂洗衣液能够去溃、除菌,对白色织物的去渍效果尤佳。同学们在对其研究时发现其中含有过氧化氢,查阅资料后得知过氧化氢溶液具有漂白性,可漂白一些有色物质,实验小组对过氧化氢的性质进行了探究。
Ⅰ.不稳定性
过氧化氢在常温下便能分解,因此盛放过氧化氢溶液的试剂瓶内壁会有一些微小的气泡,其发生反应的化学方程式是_______________,实验小组的同学向该过氧化氢溶液中加人了少量氧化铁,发现产生气泡的速度变快了,该实验_______(能、不能)说明氧化铁是过氧化氢分解的催化剂。
Ⅱ.漂白性

[提出问题]过氧化氢的漂白性与哪些因素有关?
[进行猜想]通过阅读相关资料,你认为过氧化氢的漂白性可能与________、________等因素有关。
[进行实验]
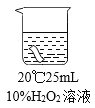
实验1:室温下用10%的过氧化氢溶液浸泡一块红色布条,浸泡时间与布条颜色变化
如下表:
浸泡时间 | 20 min | 40min | 60 min |
布条颜色的变化 | 无明显变化 | 颜色稍变浅 | 颜色明显变浅 |
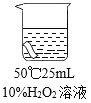
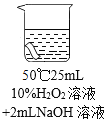
实验2:将红色布条分别浸泡在以下3种溶液中,现象如下表。
编号 | ① | ② | ③ |
实验 |
|
|
|
布条颜色 |
| 颜色稍变浅 | 颜色明显变浅 |
[解释与结论]
(1)实验1的目的是__________________。
(2)实验2中,欲得出“其它条件相同时,升高温度可使过氧化氢溶液的漂白性增强”的结论,需要对比实验_________________(填编号)。
(3)实验2中,通过对比②③得出的结论是:其它条件相同时,___________。
(4)根据上述实验,推测“使用彩漂液时水温不宜超过50C”的原因是___________________。