��Ŀ����
����Ŀ���кͷ�Ӧ�ڹ�ũҵ�������������й㷺��Ӧ�á�ij��ѧʵ��С���ͬѧ������кͷ�Ӧ�����������о���
��ʵ�����1��
����û������ʵ��������кͷ�Ӧ����ϡ������ϡ����������Һ�ķ�Ӧ��Ҫ֤������֮��ȷʵ�����˻�ѧ��Ӧ����ͨ����ͼ��ʾʵ�鲽����в�����
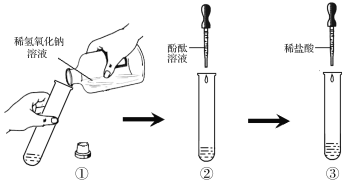
�������ͼ��ʾʵ�鲽����дʵ�鱨�棺
ʵ�鲽�� | ʵ������ | ʵ����� |
�����Թ��м���1��2mlϡ����������Һ | NaOH��HCl �������кͷ�Ӧ | |
��_______________ | ______________ | |
��____________ | ______________ |
��ʵ�����2��
����ijЩ����������������кͷ�Ӧ����ϡ���������������ķ�Ӧ���۲쵽��___�����Ϳ���˵���кͷ�Ӧ�Ѿ��������÷�Ӧ�Ļ�ѧ����ʽΪ_____������ ʾ�����������Dz�����ˮ�İ�ɫ�������仯ѧʽΪAl(OH)3��
��ʵ�鷴˼��
��1����ͬѧ���Ҳ����ʹ��ʯ����Һ�����̪��Һ���У�ʵ�����1����ʵ�顣����Ϊ______�����̪��Һ����ʯ����Һ�������ʺ�������֤ϡ������ϡ����������Һ�����кͷ�Ӧ�����������_____��
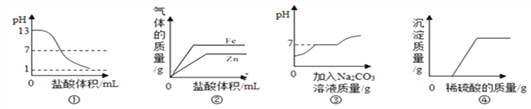
��2������û������������ֵ�����кͷ�Ӧ�����ǿ��Խ���_____�ı仯�����ж��Ƿ�Ӧ��Ӧ���еij̶ȡ�
���𰸡� ������ٵ��Թ��е��뼸�η�̪��Һ���� ��Һ����ɫ��Ϊ��ɫ ������ڵ��Թ�����������ϡ���ᣬ�� ��Һ�ɺ�ɫ��Ϊ��ɫ ��ɫ�������ܽ� Al(OH)3+ 6HCl= AlCl3 +3H2O ��̪��Һ ��ɫʯ����Һ������Һ��������������Һ���ϣ��Ӿ��۲첻�����ԣ��𰸺������ɣ� ���ָʾ����ɫ�����̪��Һ��ɫ��ʯ����Һ��ɫ��
��������
ϡ������ϡ����������Һ�ķ�Ӧû�����Ե�ʵ��������ͨ�����������������ɻ��߷�Ӧ����ʧ֤�������˷�Ӧ��
��1�����Թ��м���1��2mlϡ����������Һ֮�������Թ��е��뼸�η�̪��Һ�����۲쵽��Һ��죬˵����Һ�ʼ��ԣ�������ڵ��Թ�����������ϡ���ᣬ����Һ�ɺ�ɫ��Ϊ��ɫ��˵����Һ�����Ի������ԣ���֤���������ƺ����ᷢ���˷�Ӧ����2�����������Dz�����ˮ�İ�ɫ���壬��������֮���ܹ�������Ӧ���۲쵽��ʵ�������ǰ�ɫ�������ܽ⣬������Ӧ�Ļ�ѧ����ʽ��Al(OH)3+ 6HCl= AlCl3 +3H2O����3������̪��Һ����ʯ����Һ�����dz��������ָʾ�����������ԡ����Ե���Һ���Գ��ֲ�ͬ����ɫ����Ƚ϶��Է�̪��Һ���ʺ�������֤ϡ������ϡ����������Һ�����кͷ�Ӧ����Ϊ��ɫʯ����Һ������Һ��������������Һ���ϣ��Ӿ��۲첻�����ԣ���4������û������������ֵ�����кͷ�Ӧ�����ǿ��Խ������ָʾ����ɫ�ı仯�����ж��Ƿ�Ӧ��Ӧ���еij̶ȡ�

����Ŀ��������ֵ���ijʵ��С���ڿ���������һ��̽��ʵ��:
(1)��a�Թ��м���Լ2mL����ͭ��Һ��Ȼ����뼸������������Һ,�۲쵽��������_____��
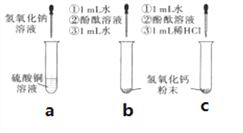
(2)��b��c��֧�Թ��и�����������ͬ�������������Ʒ�ĩ��Ȼ�������1mLˮ,��,�ʻ���״������,�ٸ�����1~2 �η�̪��Һ,�۲쵽���Թ���Һ����졣������b�Թ��м���Լ1mLˮ������c�Թ��м���Լ1mLϡ����,������b�Թܱ��������Һ�Գʺ�ɫ��c�Թܱ����,��Һ�����ɫ����b�Թ��еڶ��μ���Լ1mLˮ��������________��
��������⣩�Թ�c�м���Լ1mLϡ�����,��Һ�е�������ʲô?
����������������������CaCl2��Һ�����ԡ�
��������裩С��������I.CaCl2 ��.CaCl2��HCl ��.CaCl2��Ca(OH)2
����˼���ɣ�С���Բ���������������������___________
������ʵ�飩С��ͬѧͨ������,�������ʵ�鷽��������֤:
ʵ�鲽�� | ʵ������ | ʵ����� |
ȡ����c�Թ��е���Һ���Թ���,_______ | ________ | ���������� |
ʵ�����,С��ͬѧ��a��b��c��֧�Թ��е�ʣ�����ʻ��,���ַ�Һ�ʻ��ǡ�
�������뽻������Һ�д������ڵ���������_______��д����Һ�п��ܷ�����Ӧ��һ����ѧ����ʽ________��