题目内容
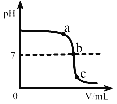
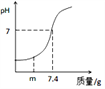
【题目】用熟石灰中和一定量的盐酸时,溶液的pH与加入的熟石灰质量的关系如图所示。写出该反应的化学方程式____________。当加入熟石灰mg时,溶液中的溶质为____________。若改用7.4g氢氧化钠与相同量盐酸反应,所得溶液的pH_________7。(填“>”、“<”或“=”)。
【答案】 Ca(OH)2+2HCl![]() CaCl2+2H2O HCl和CaCl2 <
CaCl2+2H2O HCl和CaCl2 <
【解析】
根据图像可知,加入7.4g熟石灰时,熟石灰与盐酸恰好反应。
酸碱反应生成盐和水,Ca(OH)2+2HCl![]() CaCl2+2H2O。当加入熟石灰mg时,溶液的pH<7,即盐酸剩余,所以溶液中的溶质是HCl和CaCl2。由图像可知,7.4g氢氧化钙与盐酸恰好反应,所得溶液的pH=7。设与7.4g熟石灰反应的稀盐酸中溶质的质量为x,
CaCl2+2H2O。当加入熟石灰mg时,溶液的pH<7,即盐酸剩余,所以溶液中的溶质是HCl和CaCl2。由图像可知,7.4g氢氧化钙与盐酸恰好反应,所得溶液的pH=7。设与7.4g熟石灰反应的稀盐酸中溶质的质量为x,
Ca(OH)2+2HCl![]() CaCl2+2H2O
CaCl2+2H2O
74 73
7.4g x
![]() =
= ![]() ,解得x=7.3g
,解得x=7.3g
设与稀盐酸中的7.3g溶质反应的氢氧化钠的质量是y
NaOH + HCl == NaCl + H2O
40 36.5
y 7.3g
![]() =
=![]() ,解得y=8g
,解得y=8g
所以用7.4g氢氧化钠与相同量盐酸反应时,盐酸有剩余,故所得溶液的pH<7。

 名校课堂系列答案
名校课堂系列答案【题目】FeCl2溶液中混有少量的CuCl2,为了除去CuCl2,某课外小组同学取该溶液50g于烧杯中,然后等量分5次加入某物质M充分反应,所得数据如下表,请根据相关知识和数据回答下列问题:
次数 | 1 | 2 | 3 | 4 | 5 |
加入M的质量(g) | 0.28g | 0.28g | 0.28g | 0.28g | 0.28g |
溶液的总质量(g) | 49.96 g | 49.92 g | 49.88g | 49.84g | 49.84g |
(1)写出物质M的化学式______.
(2)参加反应M的总质量是________?
(3)FeCl2溶液中CuC12的质量分数是_______?
【题目】中和反应在工农业生产和生活中有广泛的应用。某化学实验小组的同学对酸碱中和反应进行了如下研究。
(实验过程1)
对于没有明显实验现象的中和反应,如稀盐酸与稀氢氧化钠溶液的反应,要证明它们之间确实发生了化学反应,可通过下图所示实验步骤进行操作。
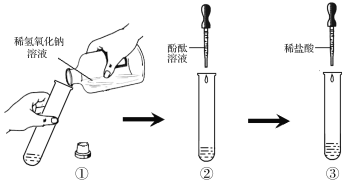
请根据上图所示实验步骤填写实验报告:
实验步骤 | 实验现象 | 实验结论 |
①向试管中加入1~2ml稀氢氧化钠溶液 | NaOH与HCl 发生了中和反应 | |
②_______________ | ______________ | |
③____________ | ______________ |
(实验过程2)
对于某些有明显现象产生的中和反应,如稀盐酸与氢氧化铝的反应,观察到有___的现象,就可以说明中和反应已经发生。该反应的化学方程式为_____。〔提 示:氢氧化铝是不溶于水的白色固体,其化学式为Al(OH)3〕
(实验反思)
(1)有同学提出也可以使用石蕊溶液代替酚酞溶液进行(实验过程1)的实验。你认为______(填“酚酞溶液”或“石蕊溶液”)更适合用于验证稀盐酸与稀氢氧化钠溶液发生中和反应,你的理由是_____。
(2)对于没有明显现象出现的酸碱中和反应,我们可以借助_____的变化,来判断是否反应或反应进行的程度。