题目内容
【题目】某品牌矿泉水,其外包装上部分文字说明如图所示,请回答下列问题。

(1)标出偏硅酸(H2SiO3)中硅元素的化合价_______;
(2)25℃时,该矿泉水呈_____________(填“酸性”、“中性”或“碱性”);
(3)硫酸镁的相对分子质量为____________;
(4)饮用这样的一瓶(300mL)矿泉水可以补充_________mg的镁元素。
【答案】 +4 碱性 120 144
【解析】本题考查了标签上标示的物质成分及其含量,有关元素化合价的计算,溶液酸碱性与pH的关系,根据化学式的计算等。
(1)化合物中,氢元素显+1价,氧元素显-2价,设:硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×3=0,则x=+4价;
(2)该矿泉水的pH>7,显碱性;
(3)硫酸镁的相对分子质量=24+32+16×4=120;
(4)300mL矿泉水中硫酸镁的质量=300mL×240mg/100 mL=720mg;
饮用这样的一瓶(300mL)矿泉水可以补充镁元素质量=720mg×![]() ×100%= 144 mg。
×100%= 144 mg。

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案【题目】碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺流程如下:
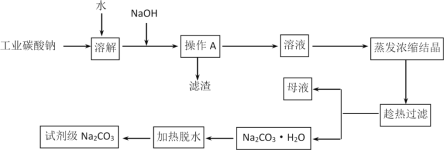
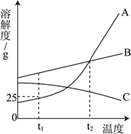
碳酸钠的饱和溶液在不同温度下析出的溶质如下表所示:
温度(℃) | ﹤32 | 32~36 | ﹥36 |
析出物的化学式 | Na2CO3·10H2O | Na2CO3·7H2O | Na2CO3·H2O |
回答下列问题:
(1)操作A为过滤,所需的玻璃仪器有烧杯、玻璃棒和_____________,滤渣的主要成分为Fe(OH)3、Mg(OH)2和___________。
(2)“趁热过滤”的原因是____________________。
(3)“母液”中除了含有 Na+、CO32-、Cl-、OH-离子外,还含有________等离子(写出一个即可)。
(4)写出Na2CO3·H2O转化为Na2CO3的化学方程式_______________________________________。
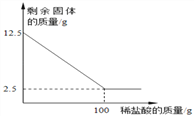
【题目】一些骗子常用黄铜冒充黄金骗取钱财,某同学通过查阅资料得知黄铜是锌和铜的合金,他取一定量的某黄铜样品放入烧杯中,再向其中分4次加入等质量的同一稀硫酸,每次均充分反应。实验过程中有关物质的用量及质量测定记录如下表:
实验次数 | 1 | 2 | 3 | 4 |
稀硫酸的用量/g | 20 | 20 | 20 | 20 |
剩余固体的质量 | 10 | 8.7 | 7.4 | 7.2 |
分析表中数据,完成下列问题:
(1)所取黄铜样品的质量为___________ g;
(2)第4次实验结束后溶液的pH __________7(填“>”、“=”或“<”);
(3)所用稀硫酸中溶质的质量分数为________________?(要求有解答过程)
【题目】中和反应在工农业生产和生活中有广泛的应用。某化学实验小组的同学对酸碱中和反应进行了如下研究。
(实验过程1)
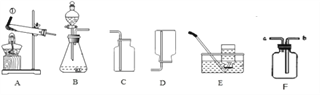
对于没有明显实验现象的中和反应,如稀盐酸与稀氢氧化钠溶液的反应,要证明它们之间确实发生了化学反应,可通过下图所示实验步骤进行操作。
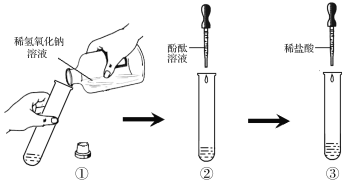
请根据上图所示实验步骤填写实验报告:
实验步骤 | 实验现象 | 实验结论 |
①向试管中加入1~2ml稀氢氧化钠溶液 | NaOH与HCl 发生了中和反应 | |
②_______________ | ______________ | |
③____________ | ______________ |
(实验过程2)
对于某些有明显现象产生的中和反应,如稀盐酸与氢氧化铝的反应,观察到有___的现象,就可以说明中和反应已经发生。该反应的化学方程式为_____。〔提 示:氢氧化铝是不溶于水的白色固体,其化学式为Al(OH)3〕
(实验反思)
(1)有同学提出也可以使用石蕊溶液代替酚酞溶液进行(实验过程1)的实验。你认为______(填“酚酞溶液”或“石蕊溶液”)更适合用于验证稀盐酸与稀氢氧化钠溶液发生中和反应,你的理由是_____。
(2)对于没有明显现象出现的酸碱中和反应,我们可以借助_____的变化,来判断是否反应或反应进行的程度。