题目内容
【题目】教材中“分解过氧化氢制氧气的反应中二氧化的化作用”,以及“寻找新的催化剂”研究性实验,引起了化学研究小组同学们的兴趣。
(提出疑问)氧化铁能否作过氧化氢溶液分解的能化剂?如果能,其效果加何?
实验步骤 | 实验现象 |
①分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生气泡,带火星的木条复燃;B试管中无明显现象 |
②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象 | 试管中均产生气泡,带火星的木条均复燃 |
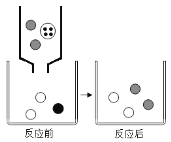
③将实验②中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
④分别量取_____过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(实验结论)(1)A中产生的气体是_____。
(2)实验2、3证明:氧化铁的质量和_____在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(3)实验4的步骤中应填写_____。
(4)写出氧化铁催化过氧化氢分解的化学反应文字表达式_____。
(实验评价)(5)设计实验4的目的是_____。
(6)若实验4观察到D试管中产生气泡的速率更快,由此可以得到的结论是_____。
(表达与交流)(7)小组同学在常温下,将a、b、c三个试管中分别加入等量5%过氧化氢的溶液,在其他条件相同时,各滴2滴5%、10%、20%的硫酸铜溶液。绘制了产生的氧气体积和时间变化的曲线如图,请你回答:
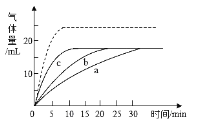
①写出两条规律性结论:_____、_____。
②若实验中所得的曲线如图中虚线所示,请推测其中可能的原因_____。
【答案】氧气 化学性质 5mL5% ![]() 氧化铁与二氧化锰哪一个更适合做过氧化氢分解生成氧气的催化剂 二氧化锰更适合做过氧化氢分解生成氧气的催化剂 硫酸铜溶液的浓度越大,过氧化氢分解的速率越大 硫酸铜溶液的浓度不会影响最终产生的氧气质量 其他条件相同时,过氧化氢溶液的浓度变大
氧化铁与二氧化锰哪一个更适合做过氧化氢分解生成氧气的催化剂 二氧化锰更适合做过氧化氢分解生成氧气的催化剂 硫酸铜溶液的浓度越大,过氧化氢分解的速率越大 硫酸铜溶液的浓度不会影响最终产生的氧气质量 其他条件相同时,过氧化氢溶液的浓度变大
【解析】
氧气具有助燃性,能使带火星木条复燃,氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂,氧化铁催化过氧化氢分解生成水和氧气。
[提出疑问] 氧化铁催化过氧化氢分解生成水和氧气, 氧化铁的质量和化学性质在反应前后均没有发生变化。
实验步骤 | 实验现象 |
①分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生气泡,带火星的木条复燃;B试管中无明显现象 |
②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象 | 试管中均产生气泡,带火星的木条均复燃 |
③将实验②中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
④分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
[实验结论](1)氧气具有助燃性,能使带火星木条复燃,实验现象A试管中产生气泡,带火星木条复燃,A中产生的气体是氧气。
(2)实验2、3证明:氧化铁的质量和化学性质在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(3)实验4的步骤中过氧化氢的质量分数和体相同,故应填写5mL5%。
(4)氧化铁催化过氧化氢分解生成水和氧气,反应的文字表达式为
![]() 。
。
[实验评价](5)二氧化锰也能做过氧化氢分解生成氧气的催化剂,故设计实验Ⅳ的目的是氧化铁与二氧化锰哪一个更适合做过氧化氢分解生成氧气的催化剂。
(6)若实验4观察到D试管中产生气泡的速率更快,由此可以得到的结论是二氧化锰更适合做过氧化氢分解生成氧气的催化剂。
[表达与交流](7)①根据图象可知,产生氧气的速率与硫酸铜溶液的浓度有关,浓度越大,分解速率越快,但是最终产生氧气的量相同,故结论是硫酸铜溶液的浓度越大,过氧化氢分解的速率越大;硫酸铜溶液的浓度不会影响最终产生的氧气质量。
②反应物的浓度越大,反应速率越快,产生的氧气越多;故可能的原因是在其他条件相同时,过氧化氢溶液的浓度变大。

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案【题目】某小组对H2O2溶液制取氧气进行了如下探究:
(探究一):探究不同催化剂对H2O2分解快慢的影响。
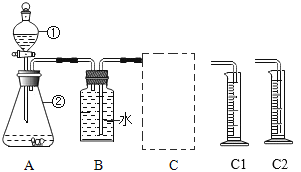
该小组采用了如图所示装置进行实验,实验中催化剂均为0.4g,H2O2溶液浓度均为10%20mL,在C框中连接导管和量筒,并测量相关数据,经计算后的数据如下表:
催化剂种类 | 气体产生速率(mL/s) |
二氧化锰 | 3.5 |
氧化铜 | 4.5 |
活性炭 | 5.8 |
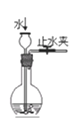
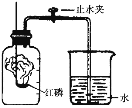
(1)实验前用弹簧夹夹住B装置右侧橡胶管,打开①的两个活塞,向其中加水,一会儿水很难流下来。这一操作步骤的目的是_____________。
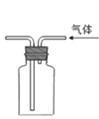
(2)为了较精确测定排出水的体积,C框内应选用的装置为_______(选填“C1”或“C2”)。
(3)实验中,可以通过测定_______(选填字母)进行探究。
A 产生相同体积氧气所需时间 B 产生氧气的总质量 C 产生氧气的总体积
(4)从实验数据可知:相同条件上表中催化剂的催化效果最好的是__________。
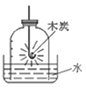
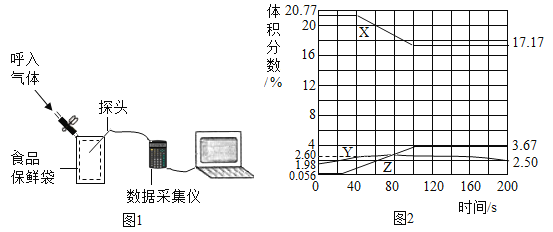
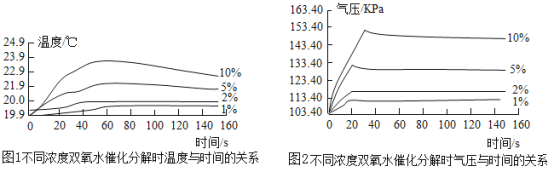
(探究二):探究H2O2溶液浓度对分解速率的影响按如图装置进行实验:水浴温度控制在18℃,在250mL三颈瓶中加入MnO2均为0.5g,在恒压漏斗中加入不同浓度的H2O2溶液各5mL分别进行实验。数字传感器数据绘制图象如下图1、图2所示。
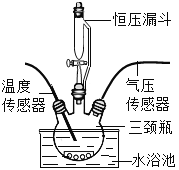
(5)实验中,恒压漏斗的作用是________
(6)由图1知道:H2O2溶液分解时__________热量(选填“放出或“吸收”)。
(7)由图2知道:H2O2溶液浓度越高,其分解反应速率越_______(选填“快”或“慢”),以10%H2O2溶液为例,约30S后三颈瓶内气压由高缓慢降低的原因是_____________。
【题目】以下是某研究小组探究影响反应速率部分因素的相关实验数据。
实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液体积/mL | 温度/℃ | 二氧化锰的用量/g | 收集氧气的体积/mL | 反应所需的时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 20 | 2 | 49.21 | |
④ | 30 | 5 | 20 | 2 | 10.76 |
(1)通过实验①和②对比可知,化学反应速率与_____________有关;从实验③和④对比可知,化学反应速率与温度的关系是_____________;
(2)用一定量15%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,则产生氧气的总重量将_____________(选填“减小、不变或增大”);
(3)写出实验②中反应的符号表达式:_____________。