题目内容
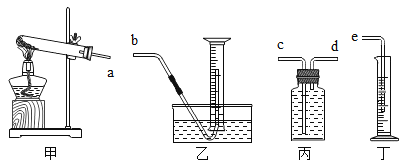
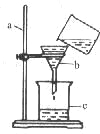
【题目】某小组对H2O2溶液制取氧气进行了如下探究:
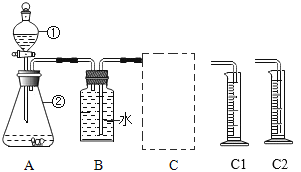
(探究一):探究不同催化剂对H2O2分解快慢的影响。
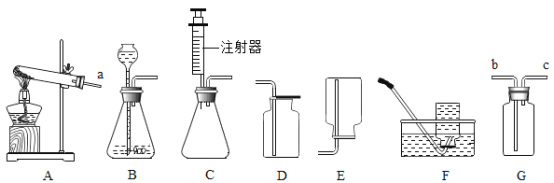
该小组采用了如图所示装置进行实验,实验中催化剂均为0.4g,H2O2溶液浓度均为10%20mL,在C框中连接导管和量筒,并测量相关数据,经计算后的数据如下表:
催化剂种类 | 气体产生速率(mL/s) |
二氧化锰 | 3.5 |
氧化铜 | 4.5 |
活性炭 | 5.8 |
(1)实验前用弹簧夹夹住B装置右侧橡胶管,打开①的两个活塞,向其中加水,一会儿水很难流下来。这一操作步骤的目的是_____________。
(2)为了较精确测定排出水的体积,C框内应选用的装置为_______(选填“C1”或“C2”)。
(3)实验中,可以通过测定_______(选填字母)进行探究。
A 产生相同体积氧气所需时间 B 产生氧气的总质量 C 产生氧气的总体积
(4)从实验数据可知:相同条件上表中催化剂的催化效果最好的是__________。
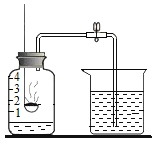
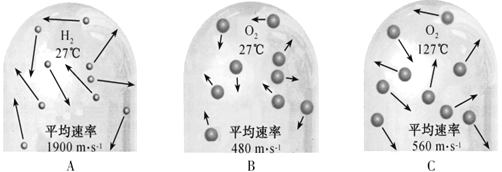
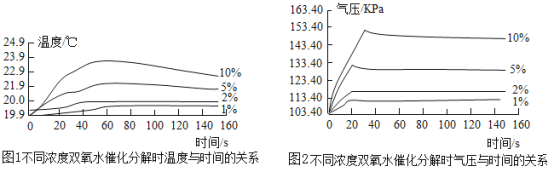
(探究二):探究H2O2溶液浓度对分解速率的影响按如图装置进行实验:水浴温度控制在18℃,在250mL三颈瓶中加入MnO2均为0.5g,在恒压漏斗中加入不同浓度的H2O2溶液各5mL分别进行实验。数字传感器数据绘制图象如下图1、图2所示。
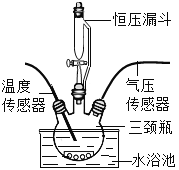
(5)实验中,恒压漏斗的作用是________
(6)由图1知道:H2O2溶液分解时__________热量(选填“放出或“吸收”)。
(7)由图2知道:H2O2溶液浓度越高,其分解反应速率越_______(选填“快”或“慢”),以10%H2O2溶液为例,约30S后三颈瓶内气压由高缓慢降低的原因是_____________。
【答案】检查装置气密性 C1 A 活性炭 平衡压强,使过氧化氢溶液顺利下滴 放出 快 30s反应结束,放热停止,随着装置冷却,三颈瓶内气压由高缓慢降低
【解析】
(1)制取气体的实验,连接好装置后要检查装置的气密性,实验前用弹簧夹夹住B装置右侧橡胶管,打开①的两个活塞,向其中加水,一会儿水很难流下来。这一操作步骤的目的是检查装置气密性。
(2)为了较精确测定排出水的体积,C框内应选用的装置为C1,防止因为导气管浸入水中而有误差。
(3)为了比较化学反应速率的快慢,该实验中,可以通过测定产生相同体积氧气所需的时间进行探究,故选A。
(4)上表中相同条件下,活性炭产生氧气的速率最快,故催化剂的催化效果最好的是活性炭。
(5)实验中,恒压漏斗的作用是使平衡压强,使过氧化氢溶液顺利下滴。
(6)由图1知道,随着反应的进行,温度逐渐升高,说明H2O2溶液分解时放出热量。
(7)由图2知道:H2O2溶液浓度越高,装置内气压越大,说明装置内气体增多,即H2O2溶液浓度越高,其分解反应速率越快,以10%H2O2溶液为例,约30S后三颈瓶内气压由高缓慢降低的原因是30s时反应结束,放热停止,随着装置冷却,三颈瓶内气压由高缓慢降低。

 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案【题目】教材中“分解过氧化氢制氧气的反应中二氧化的化作用”,以及“寻找新的催化剂”研究性实验,引起了化学研究小组同学们的兴趣。
(提出疑问)氧化铁能否作过氧化氢溶液分解的能化剂?如果能,其效果加何?
实验步骤 | 实验现象 |
①分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生气泡,带火星的木条复燃;B试管中无明显现象 |
②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象 | 试管中均产生气泡,带火星的木条均复燃 |
③将实验②中的剩余物小心过滤,并将所得虑渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
④分别量取_____过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(实验结论)(1)A中产生的气体是_____。
(2)实验2、3证明:氧化铁的质量和_____在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
(3)实验4的步骤中应填写_____。
(4)写出氧化铁催化过氧化氢分解的化学反应文字表达式_____。
(实验评价)(5)设计实验4的目的是_____。
(6)若实验4观察到D试管中产生气泡的速率更快,由此可以得到的结论是_____。
(表达与交流)(7)小组同学在常温下,将a、b、c三个试管中分别加入等量5%过氧化氢的溶液,在其他条件相同时,各滴2滴5%、10%、20%的硫酸铜溶液。绘制了产生的氧气体积和时间变化的曲线如图,请你回答:
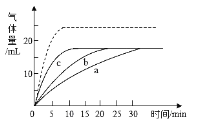
①写出两条规律性结论:_____、_____。
②若实验中所得的曲线如图中虚线所示,请推测其中可能的原因_____。